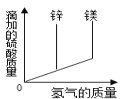
题目内容
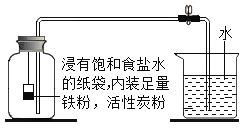
【题目】已知:碱式碳酸镁分解反应方程式为:![]() 探究小组利用下图测定xMgCO3·yMg(OH)2·zH2O组成。
探究小组利用下图测定xMgCO3·yMg(OH)2·zH2O组成。

实验步骤:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞a,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热甲中玻璃管,当乙装置中____________(填实验现象),停止加热。
步骤4:打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量。
步骤5:称量相关装置的质量。
(1)步骤④中缓缓通入空气数分钟的目的是____________。
(2)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的__________(填字母)连接在____________(填装置连接位置)。装置丁的作用是____________
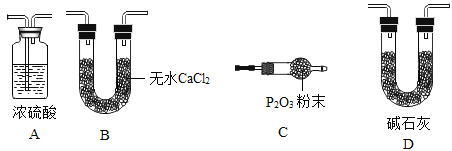
(3)若按正确装置进行实验,测得如下数据:
A 反应前玻璃管的质量100.0g
B 反应后玻璃管与残留固体总质量120.0g
C 装置乙实验后增重9.0g
D 装置丙实验后增重17.6g
根据实验测定的数据,求出碱式碳酸铜(xMgCO3·yMg(OH)2·zH2O)中x:y:z=____________
【答案】不再有气泡产生时 将甲装置产生的CO2与H2O全部排入乙与丙装置中而吸收 D 装置甲前(或a前) 防止空气中的CO2与H2O进入装置内 4:1:4
【解析】
(1)加热甲中玻璃管,当乙装置中不再有气泡产生时,停止加热;步骤④中缓缓通入空气数分钟的目的是将甲装置产生的CO2与H2O全部排入乙与丙装置中而吸收;
(2)因为空气中还有水和二氧化碳,为了排除干扰,在通入装置之前应该除去空气中的水和二氧化碳,所以在a前增加D装置;装置丁的作用是防止空气中的CO2与H2O进入装置内;
(3)根据数据可知,反应后生成氧化镁的质量为20.0g,二氧化碳的质量为17.6g,水的质量为9.0g,则有下列关系:
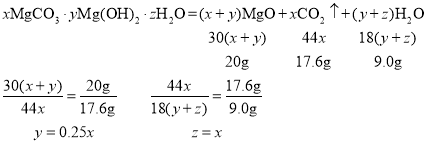
所以x:y:z=4:1:4。

【题目】我国是以煤为主要燃料的大国,北京的雾霾天气与煤作为燃料有关。煤燃烧生成的SO2是酸雨的主要污染物。
(1)工业上常以生石灰(CaO)为脱硫剂,高温下与废气中的SO2、O2化合生成CaSO4,反应方程式为________________________。
(2)某同学利用中和反应的原理模拟脱硫,将SO2通入足量KOH溶液中,并探究反应后溶液中溶质的成分。
(资料)①亚硫酸盐能使酸性KMnO4溶液褪色;②常温下,硝酸能把亚硫酸及亚硫酸盐氧化成硫酸和硫酸盐;③亚硫酸与碳酸相似,在常温下易分解。
(猜想)(Ⅰ)K2SO3;(Ⅱ)K2SO4;(Ⅲ)________________。
(进行试验)
步骤 | 实验操作 | 实验现象 | 结论 |
① | 取一定量反应后的溶液于A、B两只试管中 | ||
② | 向A试管中滴入几滴酸性KMnO4溶液。 | ________。 | 证明有K2SO3。 |
③ | 向B试管中滴入足量的稀盐酸,再加入_______。 | 有白色沉淀生成 | 证明有________。 |
(作出判断)猜想________成立。
(拓展)实验③沉淀产生的反应方程式是________________________________________。
【题目】某白色固体由BaCl2,NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组为确定其成分,进行了如下实验探究。
Ⅰ.初步探究:小金同学设计的实验过程及现象如下图所示
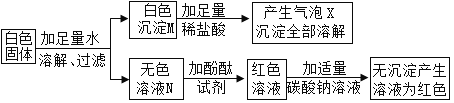
(查阅资料)BaCl2溶液显中性,BaSO4沉淀不溶于稀硝酸等酸。
(初步分析)(1)白色沉淀M的化学式是________________,产生气体X的化学方程式是_______________
(2)溶液N中的溶质一定有_____________________,一定没有氯化钡。
(3)原白色固体中一定有的物质是____________,一定没有的物质是_________________。
(交流讨论)小英同学认为:无色溶液N滴加酚酞试液后变红,说明溶液N中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠,若要进一步确定,需对溶液N继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液N中有氢氧化钠吗?
(猜想与假设)猜想1:有NaOH;猜想2:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
取无色溶液N加入过量BaCl2溶液,振荡后静置 | ______ | 证明溶液N中有碳酸钠并已被除尽 |
取上述步骤所得上层清液于试管中,加入________ | _______ | 猜想1正确 |