题目内容
【题目】自然界存在很多的化学变化。
(1)光合作用将太阳能转化为___________能。
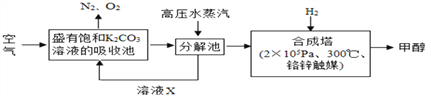
(2)打雷闪电时,空气中氧气和氮气在放电条件下,生成一氧化氮,反应化学方程式是________,NO进一步发生反应:4NO + 3X + 2H2O = 4HNO3,生成的硝酸和土壤中的矿物质生成可溶性硝酸盐,即氮肥,所以俗语说雷电发庄家,X的化学式是__________。
【答案】 化学能 N2 + O2 ![]() 2NO O2
2NO O2
【解析】本题考查了化学变化中的能量变化,化学方程式的书写和质量守恒定律的应用。
(1)光合作用将太阳能转化为化学能能。
(2)打雷闪电时,空气中氧气和氮气在放电条件下,生成一氧化氮,反应化学方程式是N2 + O2 ![]() 2NO,根据化学反应方程式4NO + 3X + 2H2O = 4HNO3可知反应后氢原子4个,氮原子4个,氧原子12个,反应前:氮原子4个,氢原子4个,氧原子6个和3X;根据质量守恒定律,在反应前后原子的种类和数目不变,3X的中氧原子的个数为6, X的化学式为O2。
2NO,根据化学反应方程式4NO + 3X + 2H2O = 4HNO3可知反应后氢原子4个,氮原子4个,氧原子12个,反应前:氮原子4个,氢原子4个,氧原子6个和3X;根据质量守恒定律,在反应前后原子的种类和数目不变,3X的中氧原子的个数为6, X的化学式为O2。

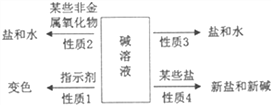
【题目】下图是一种树状分类的运用实例,下表所列的分类与下下图分类不相符的是
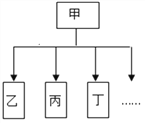
选项 | 甲 | 乙 | 丙 | 丁 | … |
A | 营养素 | 蛋白质 | 糖类 | 维生素 | … |
B | 单质 | 金刚石 | 水银 | 干冰 | … |
C | 溶液 | 碘酒 | 糖水 | 氨水 | … |
D | 化肥 | 氮肥 | 磷肥 | 钾肥 | … |
A. A B. B C. C D. D
【题目】镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I.(镍粉制备):工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体xNiCO3yNi(OH)2zH2O,并利用其制备镍粉的流程如下:
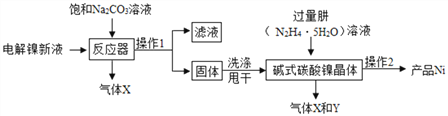
(1)反应器中一个重要反应为:3NiSO4+3Na2CO3+2H2O=NiCO32Ni(OH)2↓+3Na2SO4+2X,X的化学式为____。
(2)操作1名称是_____ , 洗涤操作1所得固体时,需用纯水洗涤,检验其洗净的方法(写出步骤、现象)___________________ 。
(3)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中95%酒精浸泡的目的 ______。
(4)物料在反应器中反应时需控制反应条件。分析下图,反应器中最适合的温度及pH分别为 ________________________ 。
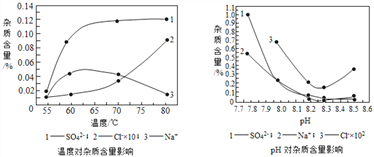
(5)生产中,pH逐渐增加,生成Ni(OH)2量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将__________填“升高”、“降低”或“不变”)。
Ⅱ.(测定碱式碳酸镍晶体的组成)
为测定碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O组成,某小组设计了如下实验方案及装置:
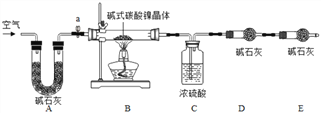
(资料卡片)
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)400℃左右,NiO会氧化生成Ni2O3.
(实验步骤):
①连接装置,_______ ;②准确称取3.77g xNiCO3yNi(OH)2zH2O放在B装置中,连接仪器;③打开弹簧夹a,缓缓鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤___________;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表)
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理):
(1)完善实验步骤中的填空:① 连接装置,_______ ;⑤___________。
(2)装置A的作用: 实验开始前、实验完毕时分别是__________________________
(3)计算xNiCO3yNi(OH)2zH2O中x:y:z的值是______________。(写出计算过程)