题目内容
【题目】CO2、O2、H2是中学化学中常见的气体,请根据下列装置图回答问题:
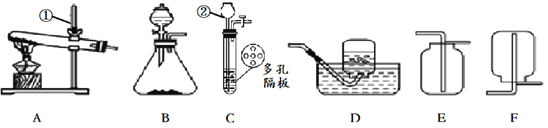
(1)写出图中仪器的名称:①___________,②_____________。
(2)实验室制取CO2的发生装置应选用________(用字母A~F填空)装置,该反应的化学方程式为_____________________。
(3)实验室用A装置制取O2的化学方程式是____________________,实验室用B装置制取O2时,加入的固体起________作用。
(4)实验室可用B装置或C装置制取H2,C装置与B装置比较的优点是_______;收集H2选用的装置是D或F,其原因是______________________。
【答案】 铁架台 长颈漏斗 B(或C) CaCO3+2HCl=CaCl2+H2O+CO2↑ 2KClO3 ![]() 2KCl+3O2↑ 催化 控制反应的发生和停止 氢气不溶于水,密度比空气小(或氢气不溶于水且不与水反应,密度比空气小且不与空气反应)
2KCl+3O2↑ 催化 控制反应的发生和停止 氢气不溶于水,密度比空气小(或氢气不溶于水且不与水反应,密度比空气小且不与空气反应)
【解析】(1)根据常见仪器解答;(2)根据碳酸钙与稀盐酸在常温下反应生成氯化钙、水、二氧化碳解答;(3)根据装置A适合于利用固体加热进行反应且试管口没有棉花解答;(4)根据C装置能控制反应的发生和停止解答;根据氢气的密度和溶解性解答。(1)图中仪器的名称:①铁架台,②长颈漏斗;(2)实验室制取CO2是碳酸钙与稀盐酸在常温下反应生成氯化钙、水、二氧化碳,应选择的发生装置是B(或C),反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;(3)装置A适合于利用固体加热进行反应且试管口没有棉花,故应选择氯酸钾和二氧化锰进行实验,反应的化学方程式为2KClO3 ![]() 2KCl+3O2↑;实验室用B装置制取O2时,加入的固体是二氧化锰,起催化作用;(4)实验室可用B装置或C装置制取H2,C装置与B装置比较的优点是能控制反应的发生和停止;收集H2选用的装置是D或F,其原因是氢气不溶于水,密度比空气小(或氢气不溶于水且不与水反应,密度比空气小且不与空气反应)。
2KCl+3O2↑;实验室用B装置制取O2时,加入的固体是二氧化锰,起催化作用;(4)实验室可用B装置或C装置制取H2,C装置与B装置比较的优点是能控制反应的发生和停止;收集H2选用的装置是D或F,其原因是氢气不溶于水,密度比空气小(或氢气不溶于水且不与水反应,密度比空气小且不与空气反应)。

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案【题目】醋酸钙和硫酸钠的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 S/g | 醋酸钙 | 36.0 | 34.7 | 33.8 | 33.2 | 33.0 | 32.7 |
硫酸钠 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
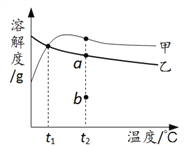
A. 甲为硫酸钠
B. t1℃应介于10℃~20℃
C. t2℃时乙溶液由b点转化到a点可恒温蒸发水或加入乙
D. 甲、乙的饱和溶液从t1℃升温到t2℃,溶质的质量分数都变小
【题目】铁及其化合物应用广泛。
(一)铁及其化合物的应用
①下图3为某小儿硫酸亚铁糖浆。
(1)适当服用该糖浆可治疗______________(选填序号)。
A.佝偻病 B.侏儒症 C.贫血症
(2)图中不涉及到的材料是_________________(选填序号)。
A.无机材料 B.合成材料 C.复合材料

②食品保鲜“双吸剂”含铁粉、食盐等,上图4为其原理探究实验:
(1)滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球______(选填“变大”、“不变”或“变小”)。
(2)食盐水的作用是______。
(二)铁及其化合物的实验
(1)将废铁屑加入滴有洗涤剂的热水中,充分搅拌以除去油污,这利用了洗涤剂的______作用。
(2)取干燥后的过量铁屑溶于一定量的稀H2SO4(水浴加热控制在50~80℃),搅拌、静置、过滤、洗涤,检验铁粉已洗净的方法是________。
(3)向上述所得滤液中加入饱和(NH4)2SO4溶液,经蒸发浓缩、________、过滤等操作得到浅蓝绿色晶体。
(查阅资料)常见含铁元素的浅蓝绿色晶体有:①硫酸亚铁晶体[FeSO47H2O];
②硫酸亚铁铵晶体[FeSO4(NH4)2SO46H2O]。
(4)取一定量晶体样品,溶于适量水,加入足量的______溶液,微热,并把产生的气体通入酚酞试液,酚酞试液变成______色,说明该晶体是硫酸亚铁铵晶体。
(三)硫酸亚铁铵晶体的热分解实验
兴趣小组称取此晶体样品39.2g,在科研人员的指导下用下图装置进行热分解实验。
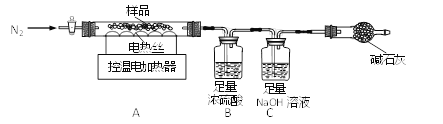
(查阅资料)①硫酸亚铁铵晶体(相对分子质量为392)在100℃完全失去结晶水,剩余物在500℃完全分解为铁的某氧化物、SO2、SO3、NH3和H2O。
②B装置中浓硫酸只能吸收NH3、SO3和H2O。
(1)装配好实验装置后,先要________。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和________。
(3)控制不同的温度对A中固体加热,测得装置B和C中的质量变化如下表。
温度/℃ | 室温 | 100 | 500 |
B装置/g | 200.00 | x | 228.00 |
C装置/g | 100.00 | 100.00 | 103.20 |
①表格中x =________。
②最终生成SO3的质量为________g,铁的某氧化物的化学式为________。
【题目】电池是日常必备用品之一,但它也是环境污染的一个重要来源。下面是某兴趣小组利用废旧锌锰干电池作为原料,并进行相关探究的过程。
(知识储备)
(1)锌锰电池的构造和组成(见图)。

(2)结晶水合物的特殊性质:在逐步升高温度条件下,结晶水合物能失去部分或者全部结晶水,如蓝色的胆矾晶体(CuSO4 5H2O)受热时可失去结晶水变为白色的无水硫酸铜粉末(CuSO4)。
I.制备皓矾晶体(ZnSO4xH2O)
小组同学参观了某回收废旧锌锰电池的工厂,其回收工艺流程如图:

(1)流程图中试剂a的化学式是________;得到的滤液1农业上可用作_______________。
(2)将滤渣B在空气中充分灼烧可提纯制得的固体是_________,该方法提纯的原理是(用化学方程式回答)______________________。
(3)测定锌皮(铜芯)中锌的质量分数:称取不同质量锌皮(铜芯)于烧杯中,并加入等浓度的稀硫酸,数据如下表所示:
锌皮(铜芯)的质量 | 20g | 15g |
稀硫酸的质量 | 100g | 120 g |
生成气体的质量 | 0.4 g | 0.4 g |
求:锌皮(铜芯)中锌的质量分数。(写出计算过程,答案保留一位小数)_______
(4)滤液2中溶质主要是硫酸锌,其有关溶解度和温度关系如下表,
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
将滤液2蒸发浓缩、_____________、过滤、洗涤、干燥,可得到皓矾晶体(ZnSO4xH2O)。
小组同学将部分皓矾晶体(ZnSO4xH2O)带回实验室,用如图装置测定晶体中结晶水的含量(图中半透膜可让气体通过又可防止固体粉末进入导管)。测定方法:称取28.7g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水:

(ZnSO4xH2O ==== ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
(5) A中的化学方程式是______________,B中的试剂可从下列物质中选取,你的选择是________。
A.浓硫酸 B.硝酸银溶液 C.饱和碳酸钠溶液 D.澄清石灰水
(6)实验过程中若不通入空气测得的结果将____________
(填“偏大”、 “偏小”或“无影响”)。根据实验结果,计算皓矾晶体中结晶水的x值为_____。
(7)将上述皓矾晶体加热会逐渐失去部分结晶水,加热过程中有关残留固体质量如右图,写出C-D
段发生反应的化学方程式____________________。