题目内容
实验室中有一包含有少量氧化铜的铜粉.同学们欲测定这包铜粉中单质铜的质量分数.现称取20g样品放入烧杯中,逐滴滴入质量分数为10%的稀硫酸至固体不再减少,共用稀硫酸49g.试计算:这包含有少量氧化铜的铜粉中单质铜的质量分数.
80%
解析试题分析:解答:解:稀硫酸中溶质的质量为49g×l0%="4.9g"
设氧化铜的质量为x.
H2SO4+CuO═CuSO4+H2O
98 80
4.9g x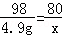
x=4g
所以混合物中铜单质的质量分数为: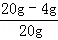 ×100%=80%
×100%=80%
答:这包含有少量氧化铜的铜粉中单质铜的质量分数是80%.
考点:根据化学反应方程式的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
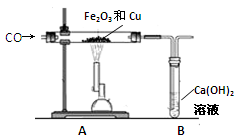
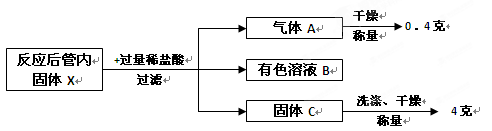
长时间使用的热水壶底部有一层水垢,主要成分是CaCO3。某校化学研究性学习小组同学通过实验想测定水垢中CaCO3的含量。他们取100g水垢,加入足量的稀盐酸,同时测量5分钟(min)内生成CO2质量,测量数据如下表:
| 时间/ min | 1 | 2 | 3 | 4 | 5 |
| 生成CO2的质量/g | 15 | 25 | 30 | 33 | 33 |
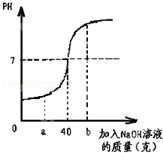
②请根据表格分析写出你发现的一条规律是 。
③该水垢中CaCO3的质量分数是多少?
Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.
(1)不法分子常用黄铜制成金光闪闪的“假元宝”蒙骗人们.下列鉴别方法中错误的是 。
| A.看颜色 | B.灼烧 | C.加硝酸银溶液 | D.加盐酸 |
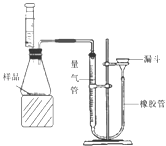
①检查装置气密性的方法是:连接好装置,从漏斗注水,量气管两边形成高度差,做好标记,一段时间后,高度差 ,说明气密性良好。
②正确读取量气管内液面的初始、最终读数前都需进行的操作是 。③该小组进行了三次实验,所得相关的实验数据处理如下:
| | 合金的质量/g | 稀硫酸的体积/mL | 生成氢气的质量/g |
| 第1次 | 2 | 15 | 0.04 |
| 第2次 | 2 | 20 | 0.04 |
| 第3次 | 4 | 15 | 0.04 |
b、分析上表数据,第 次实验,合金中的锌与稀硫酸恰好完全反应,稀硫酸的溶质质量分数为 (结果保留到0.1%)。(实验温度下,ρ(H2SO4)=1.08g/cm3)