题目内容
【题目】一包干燥的红色粉末,由 Cu 、Fe2O3 、Fe(OH)3三种固体中的一种或两种组成。下面是同学们的探究过程,请你参与并回答有关问题。
(提出猜想)
猜想①:只有 Cu
猜想②:只有Fe2O3
猜想③:只有 Fe(OH)3
猜想④:是Fe2O3 、Fe(OH)3的混合物
猜想⑤:是Cu 、Fe2O3的混合物
猜想⑥:是_______________的混合物
(查阅资料)(1)2Fe(OH)3![]() Fe2O3+3H2O
Fe2O3+3H2O
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
(实验探究)
(1)甲同学进行下列实验,请你填写表中空白处。
实验操作步骤 | 实验现象 | 结论 |
①取用少量红色固体,放于试管中加热 | ____________ | 红色固体不含Fe(OH)3 |
②取少量红色末于试管中,滴加足量稀盐酸 | 发现固体全部溶解,溶液变色 | 猜想②或猜想______成立,猜想②成立时反应的化学方程式是____________。 |
(2)在甲同学实验的基础上,乙同学为进一步确定红色粉末的组成,称取该粉末 8.0g 装入硬质玻璃管中,按如图装置进行实验。实验时发现澄清石灰水变浑浊,证明红色粉末中含有____________,硬质玻璃管中发生反应的化学方程式是________________。反应完全后测得石灰水质量增加5g(产生气体全部被稀释),则猜想_________成立。
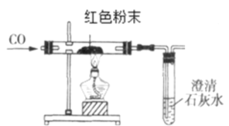
(反思评价)丙同学指出:从环保角度,乙同学的实验装置有严重不足之处。你认为改进的方法是________________。
【答案】Cu、Fe(OH)3 试管中无水雾 ⑤ Fe2O3+6HCl═2FeCl3+3H2O Fe2O3 Fe2O3+3CO![]() 2Fe+3CO2 ⑤ 尾气需要点燃
2Fe+3CO2 ⑤ 尾气需要点燃
【解析】
提出猜想:根据其他猜想,推测猜想⑥:是 Cu、Fe(OH)3的混合物;
实验探究:根据资料:2Fe(OH)3![]() Fe2O3+3H2O;而稀盐酸与氧化铁反应,生成水和氯化铁溶液,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2.;则有:
Fe2O3+3H2O;而稀盐酸与氧化铁反应,生成水和氯化铁溶液,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2.;则有:
实验操作步骤 | 实验现象 | 结论 |
①取用少量红色固体,放于试管中加热 | 试管中无水雾 | 红色固体不含Fe(OH)3 |
②取少量红色末于试管中,滴加足量稀盐酸 | 发现固体全部溶解,溶液变色 | 猜想②或猜想⑤成立,猜想②成立时反应的化学方程式是 Fe2O3+6HCl═2FeCl3+3H2O. |
(2)在甲同学实验的基础上,乙同学为进一步确定红色粉末的组成,称取该粉末8.0g装入硬质玻璃管中,按如图装置进行实验。实验时发现澄清石灰水变浑浊,证明红色粉末中含有Fe2O3;根据工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,故硬质玻璃管中发生反应的化学方程式是Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
因为反应完全后测得石灰水质量增加5g(产生气体全部被稀释)。
设:氧化铁的质量为x。
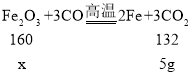
![]() ,解得x≈6.06g,则混合物中除了氧化铁,含有铜;所以猜想⑤成立。
,解得x≈6.06g,则混合物中除了氧化铁,含有铜;所以猜想⑤成立。
反思评价:一氧化碳有毒,不能直接排放到空气中,丙同学指出:从环保角度,乙同学的实验装置有严重不足之处。你认为改进的方法是尾气需要点燃。

【题目】碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业。某化学兴趣小组的同学对碳酸氢钠的性质进行了如下探究。
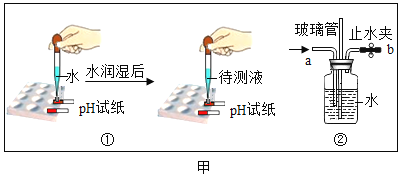
实验一:探究碳酸氢钠溶液的酸碱性用pH试纸测得碳酸氢钠溶液的pH=10,由此可知:当向碳酸氢钠溶液中滴加紫色的石蕊试液时,溶液呈_______色。
实验二:探究碳酸氢钠的热稳定性
[查阅资料]:碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
[进行实验]:为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠放到铜片上加热,如下图所示。

(1)加热一段时间后,观察到烧杯内壁有_______________。
(2)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3。
①他们猜想的依据是____________________________。
②为探究反应后的固体产物到底是NaOH还是Na2CO3,他们又进行了如下表的实验并得到结论,请你完成下表。
实 验 操 作 | 实验现象 | 结 论 |
_______________ | ____________ | 固体产物是Na2CO3 |