题目内容
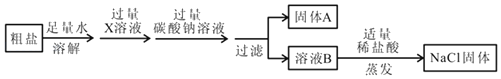
【题目】粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(CaCl2、MgCl2、Na2SO4),现以粗盐为原料制取精盐,生产流程如图所示:
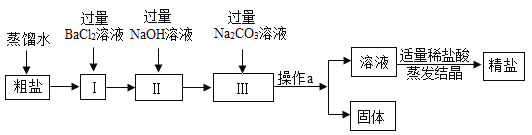
(1)在操作a中需要使用三种玻璃仪器,分别是__________________________?
(2)请写出反应I的化学方程式__________________________。
(3)加入过量Na2CO3溶液的目的是为了除去__________________离子?
【答案】漏斗、烧杯、玻璃棒 BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl Ca2+和 Ba2+
【解析】
(1)在操作a中需要使用三种玻璃仪器,分别是玻璃棒、漏斗和烧杯。
故答案为:玻璃棒、漏斗和烧杯。
(2)反应Ⅰ中,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl。
故答案为:BaCl2+Na2SO4═BaSO4↓+2NaCl。
(3)加入过量Na2CO3溶液的目的是为了除去钙离子和过量的钡离子。
故答案为:钙离子和钡离子。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象。请根据有关信息回答问题:
序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 35 | 30 | 25 | 20 | a |
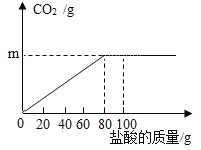
(1)a的数值为___,该品牌补钙药剂中CaCO3的质量分数是___。
(2)求该盐酸中溶质的质量分数____。(写出计算过程,计算结果保留一位小数)
(3)如果在配制该盐酸时质量分数偏小了,对该品牌补钙药剂中CaCO3的质量分数计算是否有影响。你的看法是___。
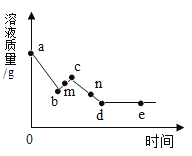
【题目】在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量关系,能用如图图像表示的是
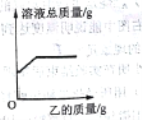
序号 | 甲 | 乙 |
① | 稀盐酸 | 金属铁 |
② | 稀硫酸 | 氢氧化铁 |
③ | 氯化钠溶液 | 硝酸银溶液 |
④ | 硝酸钾溶液 | 碳酸钠溶液 |
A.①②B.②③C.①②④D.①③④
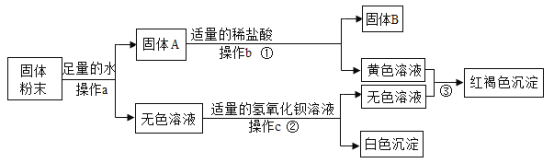
【题目】一包干燥的红色粉末,由 Cu 、Fe2O3 、Fe(OH)3三种固体中的一种或两种组成。下面是同学们的探究过程,请你参与并回答有关问题。
(提出猜想)
猜想①:只有 Cu
猜想②:只有Fe2O3
猜想③:只有 Fe(OH)3
猜想④:是Fe2O3 、Fe(OH)3的混合物
猜想⑤:是Cu 、Fe2O3的混合物
猜想⑥:是_______________的混合物
(查阅资料)(1)2Fe(OH)3![]() Fe2O3+3H2O
Fe2O3+3H2O
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
(实验探究)
(1)甲同学进行下列实验,请你填写表中空白处。
实验操作步骤 | 实验现象 | 结论 |
①取用少量红色固体,放于试管中加热 | ____________ | 红色固体不含Fe(OH)3 |
②取少量红色末于试管中,滴加足量稀盐酸 | 发现固体全部溶解,溶液变色 | 猜想②或猜想______成立,猜想②成立时反应的化学方程式是____________。 |
(2)在甲同学实验的基础上,乙同学为进一步确定红色粉末的组成,称取该粉末 8.0g 装入硬质玻璃管中,按如图装置进行实验。实验时发现澄清石灰水变浑浊,证明红色粉末中含有____________,硬质玻璃管中发生反应的化学方程式是________________。反应完全后测得石灰水质量增加5g(产生气体全部被稀释),则猜想_________成立。
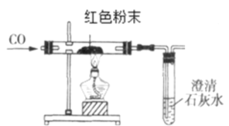
(反思评价)丙同学指出:从环保角度,乙同学的实验装置有严重不足之处。你认为改进的方法是________________。