题目内容
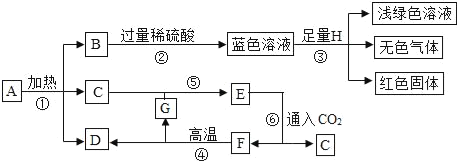
【题目】(1)根据所学知识并结合如图一所示的装置回答下列问题。
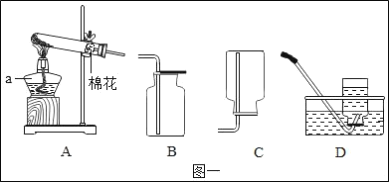
①写出标有序号的仪器名称;a_____;
②实验室选用装置A制取氧气,该反应的化学方程式为:_____;用装置D收集氧气,等到_____时开始收集,若用装置C收集氧气时,其验满方法是_____。
(2)铜片长时间露置在空气中表面会产生铜绿,为了弄清铜生成铜绿的条件及铜绿的某些性质,某实验小组进行了如下探究:
Ⅰ.探究铜生成铜绿的条件
(查阅资料)铜绿的化学式是Cu2(OH2)CO3,它受热会分解成三种氧化物。
铜绿分解的化学方程式为_____,Cu2(OH)2CO3中铜元素的化合价为_____价。
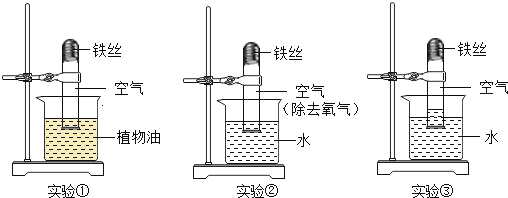
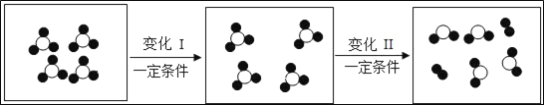
(猜想与假设)据查阅的资料和空气中含有成分的性质,实验小组依据_____定律进行判断,铜锈蚀与氮气、稀有气体无关。(设计与实验)同学们设计了“铜片锈蚀条件的探究”实验,实验如图二所示(所用铜片洁净、光亮,试管内的“![]() ”为铜片):实验较长时间后,发现_____试管中铜片最先生锈(填字母编号)。
”为铜片):实验较长时间后,发现_____试管中铜片最先生锈(填字母编号)。
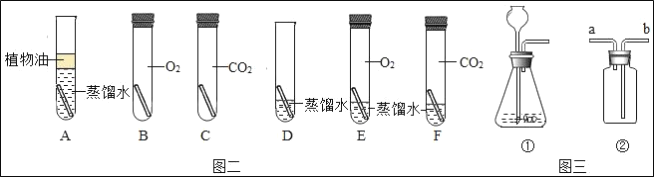
(评价与改进)小组讨论后发现
实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是:Cu和_____(写出试管中需要的物质)。
(实验结论)铜绿是铜与氧气及_____共同作用而形成的。
(拓展与应用)
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜少,他据此分析认为青铜比纯铜易锈蚀,小明的发现是否全面?请你说明理由。_____。
Ⅱ探究铜绿与盐酸的反应
实验小组取少量锏绿于装置①中,往长颈漏斗中倒人稀盐酸,观察到有气泡冒出。为检验该气体是否为CO2,应往装置②(图三)中装入适量的澄清石灰水,气体应从_____端(填“a”或“b”)进入,当出现_____的现象时,证明该气体为CO2。
【答案】酒精灯 2KMnO4![]() K2MnO4+MnO2+O2↑ 气泡连续均匀冒出 把带火星的木条放在瓶口、若木条复燃证明已集满 Cu2(OH)2CO3
K2MnO4+MnO2+O2↑ 气泡连续均匀冒出 把带火星的木条放在瓶口、若木条复燃证明已集满 Cu2(OH)2CO3![]() 2CuO+H2O+CO2 +2 质量守恒定律 D 氧气和二氧化碳 二氧化碳和水 不全面,因为不同地点空气成分的含量不同,无法比较。 b 浑浊
2CuO+H2O+CO2 +2 质量守恒定律 D 氧气和二氧化碳 二氧化碳和水 不全面,因为不同地点空气成分的含量不同,无法比较。 b 浑浊
【解析】
(1)① 由图示可知,仪器a的名称是酒精灯,故填酒精灯;
②实验室选用装置A制取氧气,试管口有一团棉花,则该反应是高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,故反应的化学方程式写为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
用装置D收集氧气,是排水法收集氧气,等到气泡连续均匀冒出时开始收集,故填气泡连续均匀冒出;
若用装置C收集氧气时,由于氧气有助燃性,其验满方法是:把带火星的木条放在瓶口、若木条复燃证明已集满,故填把带火星的木条放在瓶口、若木条复燃证明已集满。
(2)Ⅰ.{查阅资料}铜绿受热会分解成三种氧化物:氧化铜、二氧化碳和水,故反应的化学方程式写为:Cu2(OH)2CO3![]() 2CuO+H2O+CO2;
2CuO+H2O+CO2;
在Cu2(OH)2CO3中,由于氢氧根的化合价为﹣1价,碳酸根的化合价为﹣2价,根据化合物中各元素的化合价的代数和为零,可知铜元素的化合价为+2价,故填+2。
{猜想与假设}据查阅的资料和空气中含有成分的性质,实验小组依据质量守恒定律定律进行判断,铜锈蚀与氮气、稀有气体无关,故填质量守恒。
{设计与实验}实验较长时间后,发现D试管中铜片最先生锈,因为D试管中的铜与氧气、水和二氧化碳充分接触,容易生锈,故填D。
{评价与改进}由图可知实验缺少了把铜片置于装有干燥空气(或氧气和二氧化碳)的试管中,所以要补充的一个实验是:把铜片置于装有干燥空气(或氧气和二氧化碳)的试管中,放置对比观察,故填氧气和二氧化碳。
{实验结论}由上述实验的过程和现象可知,铜绿是铜与氧气及二氧化碳和水共同作用而形成的,故填二氧化碳和水。
{拓展与应用}因为不同地点空气成分的含量不同,无法比较,所以小明的分析不全面,故填不全面,因为不同地点空气成分的含量不同,无法比较。
Ⅱ、为使二氧化碳与澄清的石灰水充分接触,气体应通入石灰水中所以应从长管,即b端进入瓶中,故填b;
二氧化碳能与澄清石灰水中的氢氧化钙反应生成水和碳酸钙沉淀,使澄清石灰水变浑浊,当出现浑浊的现象时,证明该气体为CO2,故填浑浊。