题目内容
【题目】在某温度下,将A克KNO3溶液分成两等份,一份恒温蒸发水达到饱和时,质量减少一半;另一份加KNO3晶体,达到饱和时所加晶体质量恰好为该份溶液质量的1/5;在该温度下溶质的溶解度为_____g,原溶液的溶质质量分数为_____(百分号前保留整数)。
【答案】40 14%
【解析】
在某温度下,将A克KNO3溶液分成两等份,一份恒温蒸发水达到饱和时,质量减少一半,蒸发溶剂的质量是溶液质量的一半,即蒸发水的质量为![]() g×
g×![]() =
=![]() g,另一份加KNO3晶体,达到饱和时所加晶体质量恰好为该份溶液质量的
g,另一份加KNO3晶体,达到饱和时所加晶体质量恰好为该份溶液质量的![]() ,则所加晶体质量为
,则所加晶体质量为![]() g×
g×![]() =
=![]() g。
g。
将加入溶质的质量加入蒸发的溶剂质量里,会恰好达到饱和,则设t℃时A物质的溶解度是x,则![]() g:
g:![]() g=x:100g,x=40g,故填40;
g=x:100g,x=40g,故填40;
设每一份溶液中含有溶质的质量为y,则 (y+![]() ):(
):(![]() g+
g+![]() g)= y:(
g)= y:(![]() g
g![]() g)
g)
y=![]() g,原溶液的溶质质量分数为 (
g,原溶液的溶质质量分数为 (![]() g÷
g÷![]() g)×100%≈14%,故填14%。
g)×100%≈14%,故填14%。

【题目】利用传感器对二氧化碳性质再探究。
某兴趣小组利用传感器二氧化碳性质再探究.实验步骤如下:
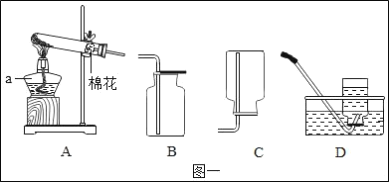
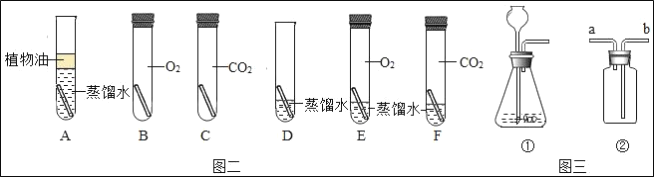
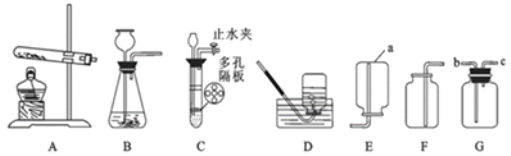
步骤1:如图1所示装置的气密性良好,三瓶:250mL的烧瓶内收集满CO2气体,三个注射器内各装有等体积的液体(分别是水、饱和石灰水、40%的氢氧化钠溶液).连接好装置和压强传感器.
步骤2:三位同学同时迅速将注射器内等体积的液体(水、饱和石灰水、40%的氢氧化钠溶液)注入各自烧瓶中,关闭活塞.
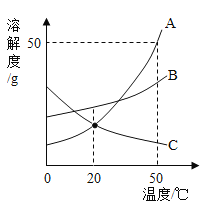
步骤3:一段时间后,同时振荡烧瓶.观察传感器定量实时地传回烧瓶内气压变化形成的图情况如图2所示.试回答下列问题:
(查阅资料)
资料1:Na2CO3+CO2+H2O==2NaHCO3
资料2:NaOH+NaHCO3==Na2CO3+H2O

(1)图1所示实验中,用“注射器”而不用“长颈漏斗”的原因是_______________________。
(2)曲线AB段气压变化的原因是______________________。
(3)导致曲线1中________段气压变化是由于充分振荡烧瓶导致的。在不改变装置药品的情况下,进一步降低E点的方法___________________。A与E几乎在一条直线上的原因是_____________________。
(4)曲线2所代表的实验中发生的反应方程式为____________________。
(5)曲线2与曲线3差异较大的原因是_____________。
(6)探究曲线3所代表的实验后的溶液中溶质的成分:
①小明同学猜想有以下六种可能:
猜想 | 一 | 二 | 三 | 四 | 五 | 六 |
成分 | Na2CO3 | NaHCO3 | Na2CO3、NaHCO3 | Na2CO3、NaOH | NaHCO3、NaOH | Na2CO3、NaHCO3和NaOH |
小新同学认为猜想五和六都是错误的,理由是___________________________。小美同学又通过计算否定了猜想二和猜想三。
②小芳同学通过实验继续探究实验
实验步骤 | 实验现象 | 实验结论 | |
取少量该实验后的溶液于试管中,滴入酚酞溶液 | 溶液呈红色 | 溶液呈________性 | 猜想四正确 |
加入________ 溶液 | _______ | 反应的化学方程式_______ | |
【题目】某兴趣小组在常温和其它相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口放置于空气中,烧杯中物质质量随时间变化如下表,请回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氯化钠浓溶液 | 氯化钙浓溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.25 | 8.47 | 10.33 |
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是______(填字母编号)。图中![]() 表示氧原子,
表示氧原子,![]() 表示氢原子
表示氢原子
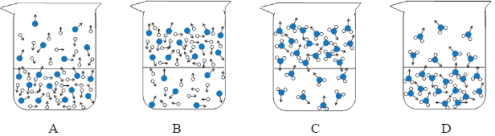
(2)为研制一种安全、环保的除湿剂,可选择上表中的(填溶质的化学式)____。
(3)现配置100g 20%的稀硫酸,则需要质量分数为98%(密度为1.84g/cm3)的浓硫酸____ml。(结果保留整数)
(4)为进一步研究稀盐酸敞口久置后浓度变化,其中甲同学猜想稀盐酸浓度可能会变大,理由是_____。