��Ŀ����
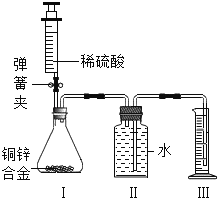
����Ŀ��Ϊ̽���������������ij��ѧ�������������ʵ�飺ȡ3�ι��������ϸ��˿���Ƴ�����״������3֧����ྻ���Թܵײ���װ����ͼ��ʾ����������ʵ�飬ʵ��Ҫ��֤���㹻����ʱ�����۲�����
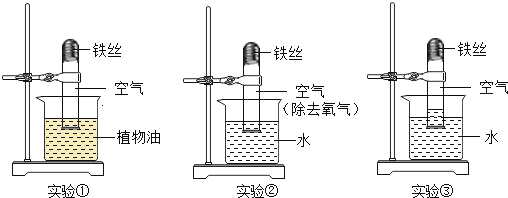
��1��������ʵ��������������е�_____�������ƣ�������Ӧ�Ľ����
��2������˿������ʱ���㹻����ʵ��۽����Թ��ڵ�ˮ�����Լռ�Թ������_____��
��3����ʵ�鴴��֮�����ڣ��ɸ�����˿����������_____�����������ж���˿��Ӧ���е������
���𰸡�ˮ������ ���֮һ �Թ���Һ������
��������
��1���Ա�ʵ��٢ڢۣ���֪������ʵ��������������е�ˮ������������Ӧ�Ľ����
��2����Ϊ����Լռ��������������֮һ������㹻��ʱ���ʵ��۽����Թ��ڵ�ˮ�����Լռ�Թ���������֮һ��
��3����ʵ�鴴��֮�����ڣ��ɸ�����˿�����������Թ���Һ�����������������ж���˿��Ӧ���е������

 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�����Ŀ��ij��ѧС�������������Ϊ���⣬������һϵ�е�ʵ��̽�����
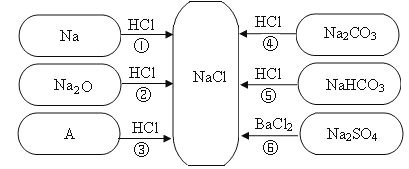
̽��1���о����������������������ƺ�����ķ�Ӧ�̶ȡ�
ʵ������ | ʵ������ | ��������� |
ȡ��Ӧ��������Һ���Թ��У�������廯����___________�� | _________ | ������� |
̽��2���о���������������ᡢ�����п��Ӧ
ͨ��̽��ʵ�飬ͬѧ�Ƿ��������������Һ�����Ժ�п��Ӧ�����������������ֹ�ͬ�����ԭ��Ϊ________________________________________________________________________��
̽��3��̽��δ֪����Ũ�����ͭ��ȡ���塣
��֪![]() ��NO2�ܺ�ˮ��Ӧ���������NO��NO��NO2���ǿ�������Ⱦ�
��NO2�ܺ�ˮ��Ӧ���������NO��NO��NO2���ǿ�������Ⱦ�
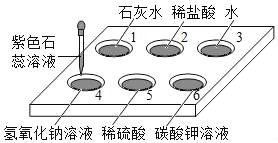
(1)���ø÷�Ӧ��ȡ���������ķ���װ�ã�Ӧѡ��ͼ��ʾװ���е�________���ռ�NO2�ķ���Ϊ________��
(2)��ӦNO��X��NO2�У�X�Ļ�ѧʽӦΪ________������Ũ�����ͭ��ȡNO��Ӧ���õ��ռ�������________________________________________________________________________��
̽��4����ȤС��ͬѧ��ʢ�г���ʯ��ˮ1000g�Ĵ��ձ��м���10g̼������Һ��ǡ����ȫ��Ӧ�����ȥ������ʣ��Һ��������Ϊ1009.8g����ô����̼������Һ��������������Ϊ________��

����Ŀ�������������ڣ�С�ܶ������ý�����������Һ��Ӧ������Ӱ��������������̽����
��������⣩���ý�����������Һ��Ӧ�Ŀ�������Щ���ص�Ӱ���أ�
����������裩a��������������Һ�����������йأ�
b���������������״�йأ�
c������������������йء�
����Ʋ�ʵ�飩С���ò�ͬ����������������Һ�Ͳ�ͬ��״��п��������ʵ�飺
ʵ���� | ������Һ��������������ȡ20mL�� | п����״ ����ȡ1g�� | �����������mL�� �����ռ�3���ӣ� |
�� | 5% | � | 15.6 |
�� | 5% | пƬ | 25.9 |
�� | 10% | � | 32.7 |
�� | 10% | пƬ | 40.9 |
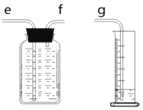
��1��С������ͼװ���ռ����������������������Ӧ��_____��ͨ�롣����e��f��g��
��2�����ռ�֤�ݣ�Ҫ�Ƚϲ�ͬ����������������Һ��п��Ӧ������Ӱ�죬����ѡ���ʵ������_____��
���ó����ۣ�����
����˼�����ۣ�����Ϊ��ʵ����ƴ�����Щ����֮��_____��