题目内容
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
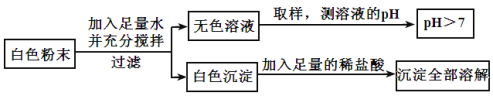
(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
【答案】CuSO4、Na2SO4 NaOH 产生白色沉淀 无色酚酞溶液 Na2CO3、BaCl2、NaOH
【解析】
硫酸铜在溶液中显蓝色,硫酸钠和氯化钡生成不溶于酸的硫酸钡沉淀,碳酸钠和氯化钡生成溶于酸的碳酸钡沉淀,氢氧化钠、碳酸钠的水溶液显碱性。
(1)白色粉末加水溶解得到无色溶液和白色沉淀,所以粉末中一定不含硫酸铜,白色沉淀加入稀盐酸,全部溶解,所以白色粉末中一定含有氯化钡、碳酸钠,一定不含硫酸钠,可能含有氢氧化钠;
(2)碳酸钠、氢氧化钠都显碱性,都能使无色酚酞变红色,要检验氢氧化钠需要先将碳酸钠检验并除去,所以
[进行实验]
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
[得出结论]白色粉末的成分是:Na2CO3、BaCl2、NaOH。

 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案