题目内容
【题目】为测定某样品(碳酸钠和氯化钠的混合物)中碳酸钠的质量分数,某化学兴趣小组进行以下实验,取50g的样品放置于烧杯中,然后取一定溶质质量分数的稀盐酸100g,加入到装样品的烧杯中,恰好完全反应得到132.4g溶液。求:
(1)样品中碳酸钠的质量分数是________(精确到0.1%)。
(2)所用稀盐酸的溶质质量分数________(写出具体的计算过程)。
(3)所得溶液的溶质质量分数________(写出具体的计算过程)。
【答案】84.8% 29.2% 41.1%
【解析】
(1)当稀盐酸质量为100g时,碳酸钠恰好与稀盐酸完全反应。生成二氧化碳的质量为:
100g+50g-132.4g=17.6g
解:设样品中碳酸钠的质量是x,盐酸中溶质的质量为y,生成的氯化钠质量为z。
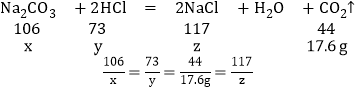
X=42.4g y=29.2g z=46.8g
(1)样品中碳酸钠的质量分数是:![]() ;
;
(2)所用稀盐酸的溶质质量分数:![]() ;
;
(3)所得溶液的溶质质量分数:![]()

 智慧小复习系列答案
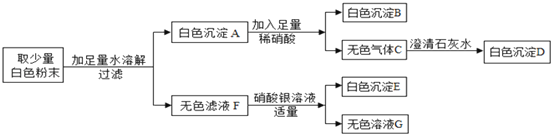
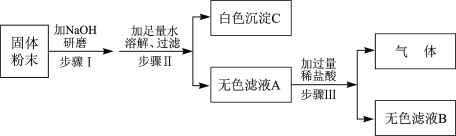
智慧小复习系列答案【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
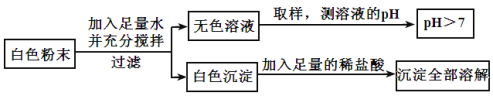
(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
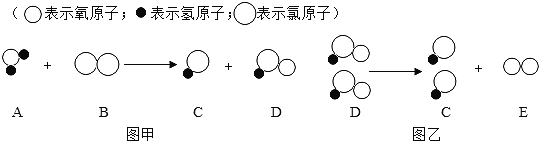
【题目】下列各组物质中,甲、乙、丙能实现如下图所示的转化关系的是(注:“→”表示反应一 步实现,部分物质和反应条件已略去)( )
甲 | 乙 | 丙 | |
① | H2O2 | O2 | H2O |
② | C | CO | CO2 |
③ | Fe | H2 | Cu |
④ | H2SO4 | HCl | HNO3 |
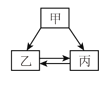
A. ①④B. ②③C. ①②D. ①②③④
【题目】如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂,甲同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到酚酞溶液不变色。
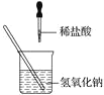
请写出该中和反应方程式:___________________________________________________。
(1)猜想与假设:
猜想一:甲同学:“两种物质已恰好完全中和,溶液呈中性”;
猜想二:乙同学:“反应后氢氧化钠过量,溶液呈碱性”;
猜想三:丙同学:__________________________________________________________。
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是:_______________________。
(2)设计并进行实验:
①为了验证自己的猜想,甲同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。 | pH________(填“>”“=”或“<”)7 | 猜想一不成立 |
②请你设计另一个实验(与甲同学方案不同)方案,验证丙同学的猜想,并填写下表:
实验步骤 | 实验现象 | 实验结论 |
__________ | __________ | __________ |
(3)拓展探究:你还能设计不同的实验方案来验证丙同学的猜想吗?
实验步骤 | 实验现象 | 实验结论 |
__________ | __________ | __________ |