题目内容
【题目】已知粗盐中含有泥沙、氯化钙和硫酸镁等杂质。为制得纯净的氯化钠固体,某化学兴趣小组进行了如下操作:
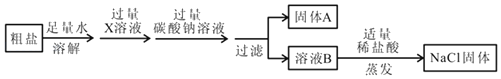
(1)写出X溶液中溶质的化学式_____。
(2)请设计实验证明溶液B中含有NaOH.(简要写出实验步骤和现象)_____
(3)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式_____。
【答案】Ba(OH)2 取少量溶液B于试管中,加入过量的CaCl2溶液,静置,取上层清液,滴加酚酞溶液,溶液变红 Na2CO3+2HCl=2NaCl+H2O+CO2↑
【解析】
(1)X溶液是氢氧化钡溶液,氢氧化钡和硫酸镁反应生成白色沉淀氢氧化镁、硫酸钡,可以除去硫酸镁,氢氧化钡的化学式是Ba(OH)2;
(2)证明溶液B中含有NaOH的方案:取少量溶液B于试管中,加入过量的CaCl2溶液,以除去碳酸钠,静置,取上层清液,滴加酚酞溶液,溶液变红,说明溶液中含有氢氧化钠;
(3)最后制得氯化钠的质量大于粗盐中氯化钠的质量,是因为稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaOH+HCl═NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑。

【题目】某小组同学在镁条与CuSO4溶液反应的实验中,除了观察到镁条上有红色物质析出,还观察到有无色无味气体产生及溶液中有沉淀生成。他们在查阅资料的基础上,针对以上实验现象进一步开展探究。

(查阅资料)
i. 氢氧化铜和碱式硫酸铜[Cu2(OH)2SO4]均难溶于水;在溶液pH < 2时,能与稀硫酸发生如下反应:
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu2 (OH)2SO4 + H2SO4 = 2CuSO4 + 2H2O
ii. 镁、铜均能与浓硝酸反应:
Mg+4HNO3=Mg(NO3)2(溶液为无色)+2NO2↑(红棕色)+2H2O
Cu+4HNO3=Cu(NO3)2(溶液为蓝色)+2NO2↑(红棕色)+2H2O
(提出假设)
I.镁条上的红色物质是金属铜。
II.无色无味气体是_____。
III.溶液中生成的沉淀可能是氢氧化铜,也可能是碱式硫酸铜或二者的混合物。
(进行实验)
序号 | 实验操作 | 实验现象及数据 | 实验结论 |
1 | 取10 mL 10% CuSO4溶液于试管中,测定 溶液pH | pH 约为3.4 | —— |
2 | 向实验1试管中加入足量打磨光亮的镁条 | 产生无色无味气体,镁条表面附着红色物质,溶液中出现沉淀 | |
3 | 将实验2中得到的附着红色物质的镁条放入试管中,加入浓硝酸 | _____ | 假设I成立 |
4 | 用小试管收集实验2中产生的气体,用拇指堵住集满气体的小试管管口,靠近酒精灯火焰,移开拇指 | 尖锐的爆鸣声,试管内壁有无色液滴 | 假设II成立 |
5 | 重复实验2,过滤、收集溶液中的沉淀,晾干,备用 | —— | —— |
6 | 取2支试管,分别标记为试管甲和试管乙,向试管甲中加入1 g_____,向试管乙中加入1 g_____;再分别向2支试管中加入5 g溶质的质量分数为10%的稀硫酸 | 试管甲中固体全部溶解,试管乙中仍有固体剩余 | 沉淀是碱式硫酸铜 |
(解释与结论)
(1)镁条与硫酸铜发生置换反应的化学方程式是_____。
(2)由实验1现象可知,CuSO4溶液呈_____(填“酸”“碱”或“中”)性。
(3)实验3中,观察到的现象是_____。
(4)根据实验4补全假设II:_____。
(5)试管甲、试管乙中加入的物质分别是_____、_____(填字母序号)。
A 氢氧化铜 B 实验5中得到的固体
(反思与评价)
(6)有同学认为根据实验6数据和现象得出“沉淀是碱式硫酸铜”结论不正确。正确的结论应为_____。