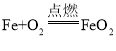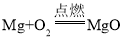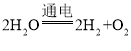题目内容
【题目】某化学课外小组对生活中另外一种常见金属铜在空气中能否生锈进行了以下探究:
[提出问题![]() 铜在空气中长期放置会生锈吗?生锈的条件是什么?
铜在空气中长期放置会生锈吗?生锈的条件是什么?
![]() 查阅资料
查阅资料![]() 铜在朝湿的空气中会慢慢生锈变绿,俗称铜绿,主要成分为碱式碳酸铜,化学式为Cu2(OH)2CO3
铜在朝湿的空气中会慢慢生锈变绿,俗称铜绿,主要成分为碱式碳酸铜,化学式为Cu2(OH)2CO3
![]() 作出猜想
作出猜想![]() (1)小组成员一致认为,铜生锈可能是铜与空气中的氧气、________共同作用的结果,他们猜想的依据是___________________。
(1)小组成员一致认为,铜生锈可能是铜与空气中的氧气、________共同作用的结果,他们猜想的依据是___________________。
![]() 设计实验
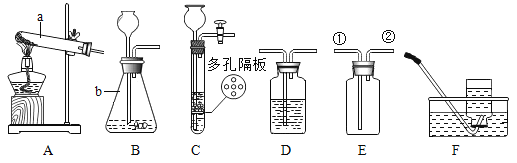
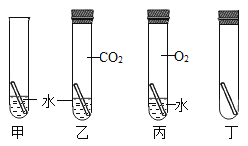
设计实验![]() 同学们设计如图实验,探究铜生锈条件:将完全相同的铜片放入不同环境中,观察生锈情况。
同学们设计如图实验,探究铜生锈条件:将完全相同的铜片放入不同环境中,观察生锈情况。
(2)小组同学讨论认为仅完成甲、乙、丙三个实验不能得出实验结论,于是又用丁试管补充了一个实验,装置中除了铜片外,还应该加入__________。
[观察现象]放置两周后,发现甲中的铜片变绿了,乙丙丁中的铜片没变化。
[得出结论]
(3)甲和乙对比,得出的结论是铜生锈需要与________接触。
(4)甲和丙对比,得出的结论是铜生锈需要与________接触。
(5)写出铜生锈生成碱式碳酸铜的的化学反应方程式是______________________。
[反思拓展]
(6)乙和丙中使用的是煮沸后迅速冷却的蒸馏水,目的是_______________________。
(7)小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由:________________。
【答案】水、二氧化碳 化学变化前后元素种类不变 二氧化碳、氧气 氧气 二氧化碳 2Cu+O2+CO2+H2O=Cu2(OH)2CO3 除去溶解在水中的氧气和二氧化碳 小明的分析不全面;因为两个铜器是从不同地点收集到的,条件不同,无法比较
【解析】
(1)由于铜锈中含有铜、碳、氢、氧,小组成员一致认为,铜生锈可能是铜与空气中的氧气、水、二氧化碳共同作用的结果,他们猜想的依据是化学变化前后元素种类不变;
(2)由甲、乙、丙的探究方法可知,装置丁中除了铜片外,还应该有二氧化碳、氧气;
(3)甲和乙对比可知,变量是氧气,得出的结论是铜生锈与氧气有关;
(4)甲和丙对比,变量是二氧化碳,得出的结论是铜生锈与二氧化碳有关;
(5)由铜生锈的条件可知,铜生锈的化学反应方程式:2Cu+O2+CO2+H2O=Cu2(OH)2CO3;
(6)由于气体的溶解度与温度有关,乙和丙中使用的是煮沸后迅速冷却的蒸馏水,原因是除去溶解在水中的氧气和二氧化碳;
(7)小明的分析不全面;因为两个铜器是从不同地点收集到的,条件不同,无法比较。

【题目】铁粉中混入了少量的某种盐杂质,为测定混合物中铁粉的质量分数,某小组进行了如下操作:称取7.7g混合物,然后将80 g稀硫酸分四次加入盛装混合物的容器中,测得加入稀硫酸的质量与生成氢气的质量关系如下表。( 盐杂质不与单质铁反应)
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/ g | 20 | 20 | 20 | 20 |
产生氢气的累计质量/g | 0.05 | 0.15 | 0.20 | m |
(1)表中m的值为______;第三次加入的硫酸________(填“被”或“未被")反应完。
(2)计算混合物中铁粉的质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)请根据数据和计算结果,在坐标中画出对应的曲线。
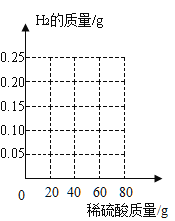
(4)第一次加入稀硫酸时,产生的氢气只有0.05g 的原因可能是________
【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的的是
编号 | ① | ② | ③ | ④ |
实验设计 |
|
|
|
|
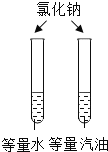
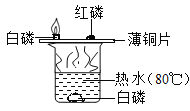
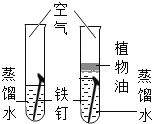
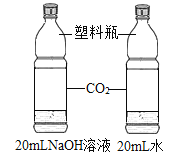
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究可燃物燃烧的条件 | 探究铁生锈的条件 | 探究CO2与NaOH溶液能否发生反应 |
A.AB.BC.CD.D