题目内容
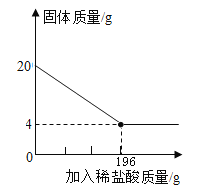
【题目】向20g某赤铁矿石(主要成分是Fe2O3,假设杂质不溶于水,也不与酸反应)样品中,逐渐加入稀硫酸,充分反应。实验相关数据如图所示。
(1)20g赤铁矿石样品中氧化铁的质量为______g
(2)计算试验中所用稀硫酸溶质的质量分数(写出计算过程)
【答案】(1)16 (2)15%
【解析】
(1)赤铁矿石与稀硫酸反应,固体减少的质量是参加反应的氧化铁的质量,根据图像可知,该赤铁矿石中氧化铁的质量为:20g-4g=16g。
⑵根据图像可知,与赤铁矿石中氧化铁恰好反应的稀硫酸的质量为196g,设196g稀硫酸中H2SO4的质量为x。
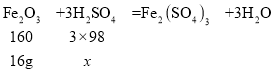
![]() ,解得x=29.4g
,解得x=29.4g
稀硫酸中溶质的质量分数为:![]() ×100%=15%
×100%=15%
答:20g赤铁矿石样品中氧化铁的质量为16g,稀硫酸中溶质的质量分数是15%。

练习册系列答案
相关题目