题目内容
【题目】酸、碱、盐是我们身边重要的化合物。
(1)碱溶液化学性质相似,因为阴离子都是___;
(2)将一定量的碳酸钠溶液与氢氧化钙溶液混合,充分反应后过滤,得到的溶液中一定含有氢氧化钠,若要验证可能含有的溶质,一定不能用的是A 酚酞溶液B 硝酸钡C 碳酸钠中的___;
(3)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:
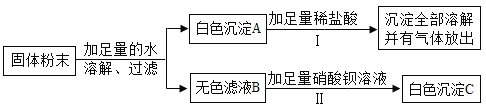
回答下列问题。
①反应I的化学方程式为_____;②白色沉淀C的化学式是_____;
③原固体粉末中一定不含____。
【答案】OH- A CaCO3+2HCl=CaCl2+CO2↑+H2O BaSO4 CuSO4、BaCl2
【解析】
(l)碱溶液中都含有氢氧根离子,故填:OH-;
(2)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,可能含有碳酸钠或是氢氧化钙,由于这三种物质都是碱性的,因此不能用酚酞试液检验,故填:A;
(3)白色沉淀A加盐酸全部溶解并且产生气体,故A是碳酸钙(一定不含有硫酸钡),由于是无色滤液,一定不含有硫酸铜,故硫酸钠和氯化钡不会同时存在,B中加入硝酸钡产生白色沉淀,说明还含有硫酸钠,故一定不会含有氯化钡;
①反应Ⅰ是碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;
②白色沉淀C是硫酸钡,故填:BaSO4;
③原固体粉末中一定不含硫酸铜和氯化钡,故填:CuSO4、BaCl2。

 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案【题目】小丽在家帮妈妈清洗碗筷,因为家里洗洁精用完了,所以妈妈告诉小丽在水中加点食用碱(主要成分![]() )也可以洗掉碗筷上的油污,小丽按照妈妈的建议把碗筷洗得干干净净。第二天的化学实验课上,小丽和同组的小明、小亮一起探究“用碳酸钠溶液清洗油污时,究竟是哪种粒子起了作用?”
)也可以洗掉碗筷上的油污,小丽按照妈妈的建议把碗筷洗得干干净净。第二天的化学实验课上,小丽和同组的小明、小亮一起探究“用碳酸钠溶液清洗油污时,究竟是哪种粒子起了作用?”
(猜想与假设)
小明猜想:水分子起了作用。
小亮猜想:________起了作用。
小丽猜想:碳酸根离子起了作用。
(进行实验)
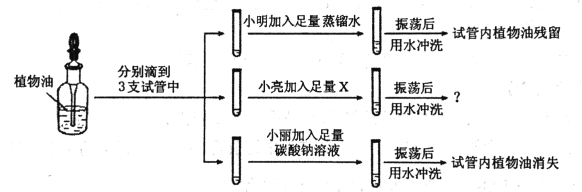
实验中小亮选用的X是________,振荡后用水冲洗,看到的现象是_________。由以上三个实验得出的结论是_________。
(反思与评价)
小明觉得上述实验的结论不准确,因为碳酸钠溶液呈碱性,溶液中一定存在________离子,很可能是这种离子起了清除油污的作用。同学们查阅资料发现:油污一般为酯类物质,在碱性条件下发生水解反应后生成可溶性的物质而使油污除去。于是他们补做了一个实验,证明小明的质疑是对的。
实验操作 | 实验现象 |
__________ | 试管内植物油消失 |
(表达与交流)
小丽告诉小组同学,食用碱在热水中溶解得快,其微观原因是_______。小亮则发现,用洗洁精与碱性溶液均可清洗油污,但二者清洗原理的不同点是______。
【题目】人类文明与社会进步同金属材料关系密切。
(一)金属的广泛应用
(1)钢铁材料通常分为生铁和钢,这两种铁合金的主要区别就在于______________。
(2)下列应用中是利用金属导热性的是_____________(填写字母序号)。

(二)金属的锈蚀及防护
(1)下列情况下铁制品最易生锈的是________________(填序号)。
a潮湿空气中 b干燥空气中 c部分浸入食盐水中
(2)写出用稀盐酸除铁锈的化学方程式______________。
(三)铁锈组成分析测定
(1)铁锈中一定含![]() ,可能含
,可能含![]() ,在某铁锈样品中加稀盐酸,_____________(填现象),证明不含
,在某铁锈样品中加稀盐酸,_____________(填现象),证明不含![]() 。
。
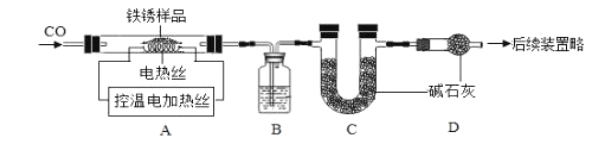
(2)另取23.2g只含![]() 的上述铁锈样品,按下图装置实验。
的上述铁锈样品,按下图装置实验。
(查阅资料)a.在110℃时,![]() 完全分解为
完全分解为![]() 和
和![]() 。
。
b.500℃时![]() 才开始被还原,且温度不同时产物可能是
才开始被还原,且温度不同时产物可能是![]() (黑色)、
(黑色)、![]() 。
。
①向装置中加入铁锈样品前,须进行的操作是________________。
②实验时,先通入CO的目的是________________。
③当加热超过500℃时,观察到A中的现象是________________。
④下表为加热至700℃时所测数据,下图为A中固体质量和加热温度关系图
反应前 | 反应后 | |
装置B/g | 100.0 | 107.2 |
装置C/g | 80.0 | 84.4 |
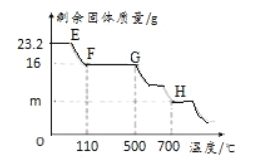
回答下列问题
a. ![]() 中n的值为________________。若无装置D,则所测n的值________________(填“
中n的值为________________。若无装置D,则所测n的值________________(填“
b. H点对应的固体为纯净物,其化学式为________________(写出计算过程)。