题目内容
【题目】某一种或几种物质的水溶液中,可能含有以下几种离子:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,现取两份溶液进行如下实验:①第一份加入
,现取两份溶液进行如下实验:①第一份加入![]() 溶液有沉淀产生。②第二份加足量的
溶液有沉淀产生。②第二份加足量的![]() 溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀部分溶解。根据上述实验,以下推测正确的是( )
溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀部分溶解。根据上述实验,以下推测正确的是( )
A.一定存在![]() B.一定存在
B.一定存在![]()
C.一定存在![]() ,可能存在
,可能存在![]() D.一定存在
D.一定存在![]() ,可能存在
,可能存在![]()
【答案】B
【解析】
(1)加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
(2)加足量Ba(NO3)2溶液后,有沉淀产生,再加入过量的稀硝酸沉淀部分溶解,说明溶液中一定有CO32-和SO42-;Ba2+与SO42-不共存,Ca2+和CO32-不共存,所以原溶液中没有Ba2+和Ca2+;又根据电荷守恒,溶液中一定有阳离子,因此一定有K+,
综上可知溶液中一定有K+、CO32-和SO42-,可能有Cl-,一定没有Ca2+、Ba2+,
故选:B。

 星级口算天天练系列答案
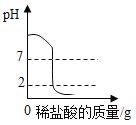
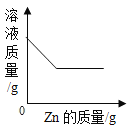
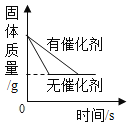
星级口算天天练系列答案【题目】下列图像能正确反映对应变化关系的是
A | B | C | D |
向一定量的氢氯化钠溶液中滴入pH=2的稀盐酸 | 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn | 硝酸铵溶于水时溶液的温度变化 | 用氯酸钾制取氧气 |
|
|
|
|
A.AB.BC.CD.D
【题目】某研究性学习小组对中和反应进行探究,请你参与实验
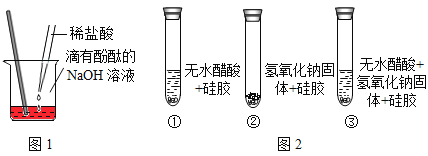
(探究活动1)证明酸和碱发生了反应
小丽同学按图1进行实验,证明了盐酸和NaOH溶液能发生化学反应,他依据的实验现象是____;反应的化学方程式____。
(探究活动2)能否通过证明有水生成来证明其反应的发生?
(设计实验)小明同学取变色硅胶、无水醋酸和氢氧化钠固体进行如图2所示的三个实验.
(小资料)a.变色硅胶吸水后由蓝色变为红色;b.无水醋酸是一种酸,常温下为无色液体;
(1)实验①、②的实验目的是____;
(2)加入试剂后,要迅速塞紧橡胶塞的原因是____;
(3)能证明酸和碱反应有水生成的现象是_____;
(4)除了上述方法之外,还可以按照下表实验方法证明稀盐酸与氢氧化钠发生了反应,说出对应的实验现象和实验结论:
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量稀盐酸,再加入少量氧化铜 | _____ | 氢氧化钠和盐酸发生了反应 |
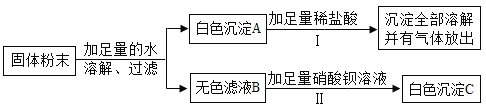
【题目】同学们整理实验室时,发现一瓶敞口放置且失去标签的白色粉末状药品,老师告诉大家原瓶药品可能是碳酸钠、碳酸钙、氢氧化钠中的一种。同学们对此很好奇,于是他们对这瓶白色粉末的成分做了如下探究:
(实验Ⅰ)小明取一定量白色粉末于烧杯中,加水搅拌,充分溶解后,过滤,得到固体和无色溶液。
(实验Ⅱ)小明取实验I得到的固体于试管中,滴加足量稀盐酸后,观察到有气泡产生,于是小明马上就得出结论,该瓶中白色粉末一定是碳酸钙,但是小军却认为小明的结论不一定正确,固体还可能是碳酸钠,小军的理由是碳酸钠溶于水形成_____(填“饱和”或“不饱和”)溶液后,也会有固体剩余。请写出碳酸钠与盐酸反应生成气体的化学方程式:_____。
(实验Ⅲ)小明和小军认为有必要再对实验I中滤液的成分进行探究,过程如下:
实验步骤 | 实验现象 | 实验结论 |
(1)取少量滤液于试管中,向其中滴加2~3滴无色酚酞溶液,振荡 | 溶液由无色变为红色 | 该瓶中白色粉末一定不是_____ |
(2)另取少量滤液于试管中,滴加过量氯化钙溶液,振荡,静置 | _____ | 该瓶中白色粉末一定有碳酸钠 |
(反思与交流)实验结束后,同学们通过讨论,一致认为原试剂瓶中的药品也可能不是碳酸钠,你认为他们的理由是_____(用化学方程式表示)。
【题目】下列实验操作、现象与结论一致的是( )
序号 | 实验操作 | 现象结论 | |
A | 向久置空气中的 | 产生气泡 |
|
B | 向某无色溶液中滴入无色酚酞试液 | 溶液变红 | 该溶液一定是碱性溶液 |
C | 将燃着的木条伸入盛满某气体的集气瓶中 | 木条熄灭 | 该气体一定是 |
D | 向某种水样中加入适量肥皂水 | 泡沫丰富 | 该水样是硬水 |
A.AB.BC.CD.D