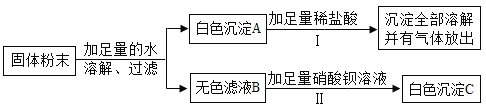
题目内容
【题目】人类文明与社会进步同金属材料关系密切。
(一)金属的广泛应用
(1)钢铁材料通常分为生铁和钢,这两种铁合金的主要区别就在于______________。
(2)下列应用中是利用金属导热性的是_____________(填写字母序号)。

(二)金属的锈蚀及防护
(1)下列情况下铁制品最易生锈的是________________(填序号)。
a潮湿空气中 b干燥空气中 c部分浸入食盐水中
(2)写出用稀盐酸除铁锈的化学方程式______________。
(三)铁锈组成分析测定
(1)铁锈中一定含![]() ,可能含
,可能含![]() ,在某铁锈样品中加稀盐酸,_____________(填现象),证明不含
,在某铁锈样品中加稀盐酸,_____________(填现象),证明不含![]() 。
。
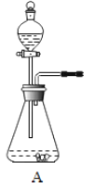
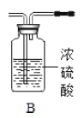
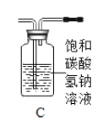
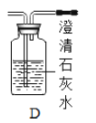
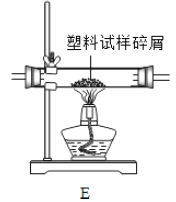
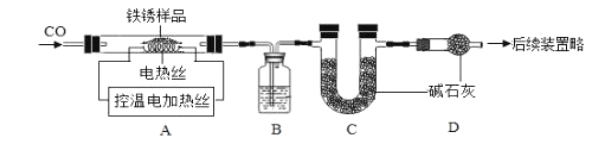
(2)另取23.2g只含![]() 的上述铁锈样品,按下图装置实验。
的上述铁锈样品,按下图装置实验。
(查阅资料)a.在110℃时,![]() 完全分解为
完全分解为![]() 和
和![]() 。
。
b.500℃时![]() 才开始被还原,且温度不同时产物可能是
才开始被还原,且温度不同时产物可能是![]() (黑色)、
(黑色)、![]() 。
。
①向装置中加入铁锈样品前,须进行的操作是________________。
②实验时,先通入CO的目的是________________。
③当加热超过500℃时,观察到A中的现象是________________。
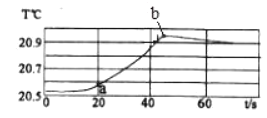
④下表为加热至700℃时所测数据,下图为A中固体质量和加热温度关系图
反应前 | 反应后 | |
装置B/g | 100.0 | 107.2 |
装置C/g | 80.0 | 84.4 |
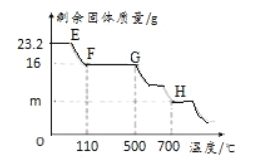
回答下列问题
a. ![]() 中n的值为________________。若无装置D,则所测n的值________________(填“
中n的值为________________。若无装置D,则所测n的值________________(填“
b. H点对应的固体为纯净物,其化学式为________________(写出计算过程)。
【答案】含碳量的不同 A C Fe2O3+6HCl=2FeCl3+3H2O 无气泡产生 检查装置的气密性 排尽装置中的空气,防止加热时发生爆炸 粉末由红棕色逐渐变成黑色 4 不变 ![]()
【解析】
(一)
(1)生铁和钢两种铁合金的主要区别就在于含碳量不同;
(2)物质的性质决定物质的用途,铁锅利用了铁的导热性,铜线利用了铜的导电性,钢丝绳,利用了铁的延展性,黄金首饰利用了金的金属光泽,故选:A;
(二)
(1)铁在有电解质存在的环境中最易发生生锈,所以铁制品最易生锈的是:部分浸入食盐水中,故选C;
(2)氧化铁和盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(三)
(1)碳酸盐和酸反应会生成二氧化碳,所以铁锈中一定含 Fe2O3nH2O,可能含 FeCO3,在某铁锈样品中加稀盐酸,不产生气泡,证明不含FeCO3;
(2)①有气体参与的反应,在实验前需要检验装置的气密性;
②可燃性气体和助燃性气体混合点燃可能发生爆炸,所以实验时,先通入CO的目的是:排装置中的空气,防止加热时发生爆炸;
③一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,所以当加热超过500℃时,观察到A中的现象是:红棕色粉末变成黑色;
④a 110℃时, ![]() 完全分解为
完全分解为![]() 和
和![]() ,由表中数据可知,反应生成水的质量为:23.2g﹣16g=7.2g,生成氧化铁的质量为16g ,则有:
,由表中数据可知,反应生成水的质量为:23.2g﹣16g=7.2g,生成氧化铁的质量为16g ,则有:
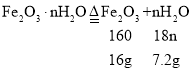
![]()
n=4;
装置D是为了防止空气中的水和二氧化碳进入C,会影响生成二氧化碳测量,不影响反应生成水的测量,若无装置D,则所测n的值不变;
b 反应生成二氧化碳的质量为:84.4g﹣80g=4.4g,
设:若反应生成FeO,参加反应的氧化铁质量为x。
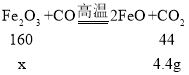
![]() x=16g 通过推导可知,700℃以上时,管内固体产物的化学式为FeO。
x=16g 通过推导可知,700℃以上时,管内固体产物的化学式为FeO。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】下列实验操作、现象与结论一致的是( )
序号 | 实验操作 | 现象结论 | |
A | 向久置空气中的 | 产生气泡 |
|
B | 向某无色溶液中滴入无色酚酞试液 | 溶液变红 | 该溶液一定是碱性溶液 |
C | 将燃着的木条伸入盛满某气体的集气瓶中 | 木条熄灭 | 该气体一定是 |
D | 向某种水样中加入适量肥皂水 | 泡沫丰富 | 该水样是硬水 |
A.AB.BC.CD.D