题目内容
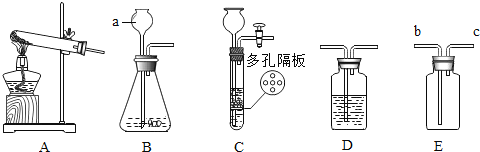
【题目】结合下列实验装置图,回答有关问题:
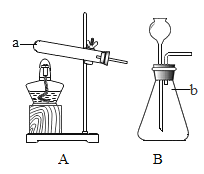
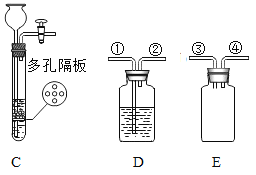
(1)仪器b的名称为_____。
(2)实验室用高锰酸钾制取氧气应选择的发生装置是_____(填字母),该反应的化学方程式为_____。
(3)对于实验室制取气体,小虹总结了如下规律,你认为正确的是_____。
a.反应必须加热 b.反应物必须是纯净物 c.生成物中只有一种气体
(4)实验室常用装置C代替B制取气体,装置C的优点是_____。
(5)如果实验室用B制取二氧化碳,用到的药品是稀盐酸和_____,该反应的化学方程式为_____,若要得到干燥的二氧化碳,应在装置D中盛放_____试剂(填试剂名称),并把气体从_____端通入。
(6)用E收集二氧化碳,从③端通入,请把装置图补画齐全_____。
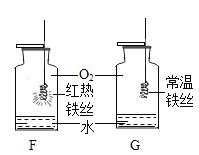
(7)制得的氧气用于图2所示的实验,发现G中铁丝不燃烧,原因是_____。
【答案】锥形瓶 A 2KMnO4![]() K2MnO4+MnO2+O2↑ c 可以控制反应的发生与结束 大理石 2HCl+CaCO3=CaCl2+H2O+CO2↑ 浓硫酸 ①
K2MnO4+MnO2+O2↑ c 可以控制反应的发生与结束 大理石 2HCl+CaCO3=CaCl2+H2O+CO2↑ 浓硫酸 ① 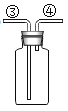 导管口未出现连续均匀气泡时就收集了氧气,氧气不纯
导管口未出现连续均匀气泡时就收集了氧气,氧气不纯
【解析】
(1)b为固液反应的装置锥形瓶;
故答案为:锥形瓶。
(2)高锰酸钾为固体,需要加热制取氧气,所以发生装置为A;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气;
故答案为:A;2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(3)a、制备二氧化碳不需要加热,a错误;
b、氯酸钾与二氧化锰、双氧水与二氧化锰、盐酸与大理石都是混合物制备气体,b错误;
c、制备气体时只能制备一种气体,否则无法达到收集纯净气体的目的,c正确;
故答案为:c。
(4)关闭止水夹,内部气体增多,压强增大,液体通过多孔隔板,被压入长颈漏斗,固液分离,反应结束;打开止水夹,气体输出,压强减小,液体重新进入试管,与固体接触,反应发生;
故答案为:可以控制反应的发生与结束。
(5)实验室选用大理石与稀盐酸制备二氧化碳,所以除了盐酸外还需要大理石;大理石主要组分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;干燥气体时利用浓硫酸的吸水性,进行干燥;为了保证气体充分流过浓硫酸,所以从①通入气体;
故答案为:大理石;2HCl+CaCO3=CaCl2+H2O+CO2↑;浓硫酸;①。
(6)二氧化碳密度比空气大,聚集在底部,所以从长口进入二氧化碳,短口排出空气,因此③为长管;
故答案为: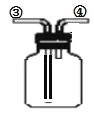 。
。
(7)铁丝不燃烧说明氧气不纯,若收集气体时,导管口未出现连续均匀的气泡就收集氧气,混入了空气,导致氧气不纯,铁丝无法燃烧;
故答案为:导管口未出现连续均匀气泡时就收集了氧气,氧气不纯。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案