题目内容
【题目】某家里蒸馒头用的纯碱中含有少量的氯化钠,某实验小组要测定该纯碱中碳酸钠的含量。现请回答将该纯碱样品8g,加入136.7g某盐酸恰好完全反应,同时产生了2.2g气体。试计算
(1)纯碱样品中碳酸钠的质量_____。
(2)反应后所得氯化钠溶液的溶质质量分数_____。
【答案】5.3g 6%
【解析】
(1)设样品中碳酸钠的质量为x,与盐酸反应生成的氯化钠为y。
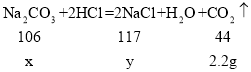
![]() ,x= 5.3g,
,x= 5.3g,
![]() ,y=5.85g
,y=5.85g
(2)溶液中氯化钠的质量=5.85g+(8g-5.3g)=8.55g,溶液的质量=8g+136.7g-2.2g=142.5g,则反应后所得氯化钠溶液的溶质质量分数=![]()
答:(1)纯碱样品中碳酸钠的质量为5.3g;
(2)反应后所得氯化钠溶液的溶质质量分数为6%。

练习册系列答案
相关题目