题目内容
【题目】教材指出:H2O2分解的催化剂并非只有二氧化锰一种。实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂。针对上述结论,南开中学初三化学兴趣小组进行了如下探究:

探究一:比较同浓度FeCl3溶液、CuSO4溶液的催化效果
(1)请写出甲图左侧试管H2O2分解的化学方程式:_____。
(2)如用图甲装置进行实验,应观察同时滴入两种溶液后_____的现象。
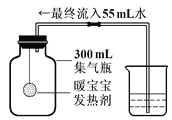
(3)如用图乙装置进行实验,实验前检查该装置气密性良好。应测量生成等体积气体时所需的_____。
(4)已知过氧化氢分解是一个放热反应。用图乙装置进行实验时,细心的小丽同学观察到,锥形瓶中不再产生气泡后注射器的活塞向左移了一小段,请你推测出现该现象的原因_____。
探究二:证明红砖粉末可以作过氧化氢分解的催化剂
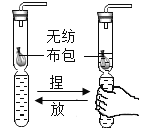
(5)小熊同学设计了如下实验:
她分别取2mL5%的H2O2溶液于两试管中,再称取0.5g红砖粉末倒入其中一支试管,发现加了红砖粉末的一支试管产生气泡速率较快。小熊认为,由此可证明红砖粉末可以作过氧化氢分解的催化剂。
小陈同学认为小熊的证明过程不够严密,需要补充下面两项实验。
实验结束后,小陈将试管内的剩余药品经①_____、洗涤、干燥后,称量得到固体质量仍为0.5g。
应补充的另一项实验为(填写实验操作)②_____。
【答案】2H2O2![]() 2H2O+O2↑ 产生气泡的快慢 时间 温度降低,装置内压强减小 过滤 将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率
2H2O+O2↑ 产生气泡的快慢 时间 温度降低,装置内压强减小 过滤 将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率
【解析】
探究一:
(1)甲图左侧试管H2O2分解的化学方程式:2H2O2![]() 2H2O+O2↑ ;
2H2O+O2↑ ;
(2)在过氧化氢分解的反应中,催化剂的作用是加快反应速率,如用图甲装置进行实验,应观察同时滴入两种溶液后产生气泡的快慢的现象,进而比较二者的催化效果;
(3)如用图乙装置进行实验,实验前检查该装置气密性良好。应测量生成等体积气体时所需的时间。时间越少,说明反应越快;
(4)已知过氧化氢分解是一个放热反应。用图乙装置进行实验时,细心的小丽同学观察到,锥形瓶中不再产生气泡后注射器的活塞向左移了一小段,出现该现象的原因反应中,由于反应放热,生成气体的温度高于室温,气体膨胀(压强增大),反应结束后,气体冷却,体积减小(压强变小);
探究二:
(5)红砖粉末是不溶固体,实验结束后,可用过滤的方法将红砖粉末分离出来,所以:将试管内的剩余药品经①过滤、洗涤、干燥后,称量得到固体质量仍为0.5g;
催化剂是能改变其他物质的反应速率而本身的质量和化学性质在反应前后都没有改变的物质,所以还应该证明红砖粉末在反应前后的化学性质没有改变。应补充的另一项实验为:将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率。如过氧化氢仍然快速分解,产生大量气泡,说明反应前后红砖粉末的化学性质没变。

 一课一练课时达标系列答案
一课一练课时达标系列答案【题目】氢氧化钠如果保存不当容易吸收空气中的二氧化碳而变质[NaOH(Na2CO3)]。某化学课外活动小组的同学,为了测定实验室因部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃、101kPa下进行。
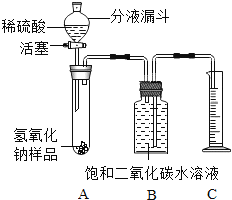
实验步骤如下:
①按图连接好装置;
②用天平准确称取氢氧化钠样品mg,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液VmL;
④计算氢氧化钠样品中碳酸钠的质量分数。
请回答下列问题:
(1)氢氧化钠发生变质的化学方程式:________。
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是_______。
(3)B中集气瓶盛装的饱和二氧化碳水溶液不能用水代替,其原因是_______。
(4)叙述检验氢氧化钠部分变质的方法:
实验步骤 | 实验现象 | 实验结论 |
①取样,溶于水,滴加过量的_______ | 产生白色沉淀 | 氢氧化钠部分变质 |
②静置,向上层清液中滴加________ | _____ |
(5)取10g变质的氢氧化钠于烧杯中,其中碳元素的质量分数为6%,向烧杯中加入100g一定质量分数的稀盐酸(足量),则反应结束后烧杯内物质的总质量是____g