题目内容
【题目】请根据下图中a、b、c三种物质的溶解度曲线,回答下列问题:
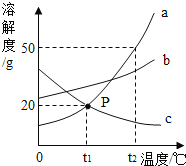
(1)P点的含义是__________。
(2)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质的质量分数由大到小的顺序是______。
(3)适合采取冷却热饱和溶液析出晶体的是______。
(4)你还能获得哪些信息(只写一条)_______。
【答案】t1℃时,a、c的溶解度相等,都为20g b>a>c a a、b的溶解度随温度的升高而增加,c的溶解度随温度的升高而减小
【解析】
(1)由图可知,t1℃时,a、c的溶解度曲线相交,故P点的含义是:t1℃时,a、c的溶解度相等,都为20g;
(2)由图可知,a、b的溶解度随温度的升高而增加,c的溶解度随温度的升高而减小,故将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,a、b还是饱和溶液,c变为不饱和溶液,t1℃时,b的溶解度大于a,故该温度下,b的饱和溶液的溶质质量分数大于a的饱和溶液的溶质质量分数,c变为不饱和溶液,降温后,溶质质量分数不变,t2℃时,c的溶解度小于t1℃时,a的溶解度,故t1℃时,a的饱和溶液的质量分数>c的溶质质量分数,故将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质的质量分数由大到小的顺序是:b>a>c;
(3)由图可知,a的溶解度受温度的影响较大,故适合采取冷却热饱和溶液析出晶体的是:a;
(4)通过溶解度曲线还能获得以下信息:t1℃时,a、c的溶解度为20g;t2℃时,a的溶解度为50g;a、b的溶解度随温度的升高而增加,c的溶解度随温度的升高而减小等。

【题目】某化学兴趣小组的同学在学习盐的化学性质时,做了如下实验:向一定量的NaHCO3溶液中加入一定量的稀HCl,反应的化学方程式是:![]() ,待完全反应后(假设反应产生的气体全部逸出),对反应后溶液的溶质成分进行如下探究。(限选试剂用品: pH试纸、镁片、稀盐酸、AgNO3溶液、氧化铜粉末、石蕊溶液)请完成猜想,并根据问题填空:
,待完全反应后(假设反应产生的气体全部逸出),对反应后溶液的溶质成分进行如下探究。(限选试剂用品: pH试纸、镁片、稀盐酸、AgNO3溶液、氧化铜粉末、石蕊溶液)请完成猜想,并根据问题填空:
(假设与猜想)
猜想1:_____________;猜想2: NaCl、 NaHCO3;猜想3: NaCl、 HCl;猜想4: NaCl、 NaHCO3、HCl。
同学们经过讨论一致认为猜想 4不成立,理由是:_______________。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
(1)取反应后溶液,加入稀盐酸 | 无气泡产生 | 猜想_________不成立 |
(2)取反应后溶液,滴在pH试纸上 | 试纸变色, 对照比色卡,pH<7 | 猜想3成立 |
(3)取反应后溶液,加入氧化铜粉末 | _______________________ | 猜想3成立,写出反应的化学方程式:______________ |
(4)取反应后溶液,滴加AgNO3溶液 | 产生白色沉淀 | 猜想3成立 |
(得出结论)猜想3正确。
(评价与反思)老师对同学们的探究过程给予了肯定,同时指出探究中存在着一处明显的错误,原因是___________________。
(总结提高)依据所给的实验用品,你还有什么不同的方案确认猜想3是正确的。请写出一种实验方案:___________________。