题目内容
【题目】小强同学在复习单质、氧化物、酸、碱、盐性质时,用铁、氧化铜、稀硫酸、氢氧化钙溶液、硫酸铜溶液五种物质,构建了如下图所示的知识网络图(图中短线“—”表示相连的两种物质能在一定条件下发生反应)。回答下列问题:
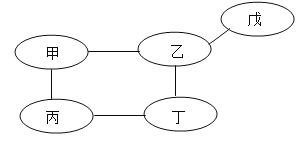
(1)戊物质是_________。
(2)丙物质属于______(填“酸”或“碱”或“盐”)。
(3)若丙和丁发生的反应属于置换反应,则此反应的化学方程式为:__________。
【答案】氧化铜或CuO 盐 Fe+CuSO4=Cu+FeSO4
【解析】
(1)乙能与三种物质反应,给出的物质中,能与三种物质反应的物质为硫酸,故乙为硫酸,不与硫酸反应的丙为硫酸铜,硫酸铜能与甲和丁反应,则甲和丁为氢氧化钠或铁,则戊为氧化铜,
(2)丙为硫酸铜,所以丙是盐类物质;
(3)若丙和丁发生的反应属于置换反应,则此反应是铁和硫酸铜反应,其反应的化学方程式为Fe+CuSO4=Cu+FeSO4。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
【题目】酸、碱、盐在我们的生活中有着重要的作用。
(1)固体氢氧化钠应当密封保存,原因是_____;_____;氢氧化钠可以做炉具清洁剂,其原理是_____。
(2)人体中碳酸氢钠可以治疗胃酸过多,该反应_____(属于或不属于)中和反应,氢氧化铝也可用于治疗胃酸过多,化学方程式为_____。
(3)某化工厂排放的废水中可能含有碳酸钾、氢氧化钾,化学兴趣小组为了确定废水中所含物质,请你设计实验进行检验_____。
(4)化学兴趣小组为探究废水中碳酸钾的含量,取50g废水样品于烧杯中,滴入的稀硫酸恰好完全反应,记录有关数据如表。请计算该废水中碳酸钾的质量_____。
反应前 | 反应后 | |
烧杯和废水的质量 | 溶质质量分数为9.8%的硫酸 | 烧杯和溶液总质量 |
60 g | 75 g | 132.8g |