题目内容
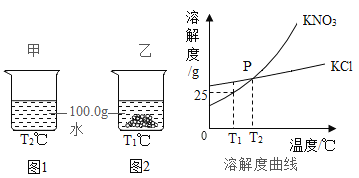
【题目】T1℃时,将等质量的KNO3、KCl分别加入到各盛有100.0g水的两个烧杯中,充分搅拌后恢复到T1℃,现象如图1、2所示。下列说法正确的是
A.甲中加入的固体是KCl
B.T1℃时,甲中溶液一定是该溶质的不饱和溶液,乙中上层清夜一定是该溶质的饱和溶液
C.将甲、乙中的物质混合,充分搅拌,一定有固体剩余
D.若将甲、乙的温度从T1℃升高到T2℃,两溶液中的溶质质量分数相等
【答案】AD
【解析】
A、在T1℃时,KNO3的溶解度小于KCl的溶解度,对比甲乙两个烧杯,没有固体剩余的甲烧杯一定加入的固体是KCl,符合题意;
B、T1℃时,甲溶液中没有固体,但不一定是该溶质的不饱和溶液,也可能是刚饱和溶液,乙中有固体剩余,所以上层清夜一定是该溶质的饱和溶液,不符合题意;
C、将甲、乙中的物质混合,充分搅拌,乙中的固体有可能溶解在甲中的溶剂中,所以混合后不一定有固体剩余,不符合题意;
D、T1℃时甲已完全溶解完,若将甲、乙的温度从T1℃升高到T2℃,两物质已完全溶解,所以两溶液中的溶质质量分数相等,符合题意。故选AD。

【题目】天然气的主要成分是甲烷(CH4),化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与探究与分析:
[提出问题]甲烷在氧气中燃烧后生成哪些物质?
[知识储备]含碳元素的物质在氧气中完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝色。
[猜想与假设]
产物猜想 | 甲 | 乙 | 丙 | 丁 |
CO2、H2O | CO、H2O | NH3、CO2、H2O | CO2、CO、H2O |
有人认为丙同学的猜想是错误的,理由是________。
[实验探究]为了验证上述猜想与假设,将4.8g甲烷在l6g氧气中燃烧的产物依次通过下列装置(假设每步都能完全吸收):
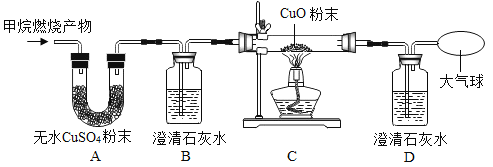
(1)A、B装置的顺序_________(填“能”或“不能”)颠倒。
(2)实验中观察到A中_________现象, 并增重________,说明有水生成。装置B增重4.4g,装置B中发生反应的化学方程式___________。
(3)装置C中观察到固体有黑色变成红色的现象,说明有______生成, 由此推断______同学猜想成立。
(4)请写出4.8g的甲烷在16g氧气中燃烧化学方程式:_______。