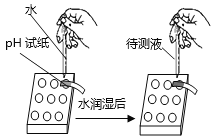
题目内容
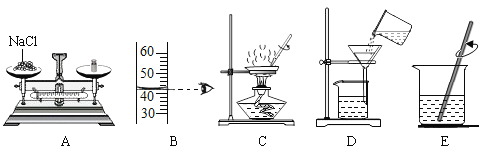
【题目】“五一”假期,聪聪同学和家人到安徽省博物馆去参观,发现博物馆内许多铜制品表面有一层绿色物质。绿色物质是什么?它是怎样形成的?化学活动课上,同学们设计实验对这种绿色物质进行了如下探究活动。
(査阅资料)
①铜在空气中易生成铜锈,它为绿色,其主要成分是Cu2(OH)2CO3;
②白色的硫酸铜粉末遇水能变为蓝色。
探究活动一:验证铜锈的组成。
(进行实验1)
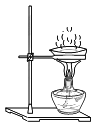
同学们设计了如图所示装置并进行实验。
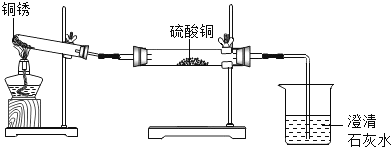
实验操作 | 实验现象 | 实验结论 |
①按如图组装仪器,装入药品。 ②加热铜锈,直至不再有气体产生,停止加热 | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊 | 加热铜锈生成的物质有_____; |
③冷却后,向试管中固体加入适量稀硫酸,稍加热 | 黑色固体溶解,溶液变为蓝色 | 发生反应的化学方程式为:_____。 |
探究活动二:探究铜生锈的条件。
(进行实验2)
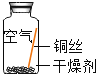
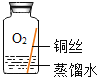
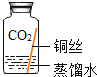
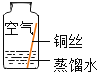
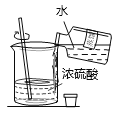
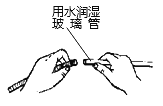
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
序号 | 实验1 | 实验2 | 实验3 | 实验4 |
实验内容 |
|
|
|
|
实验现象 | 在干燥环境中,铜不生锈 | 铜仅与氧气和水接触,不生锈 | 铜仅与二氧化碳和水接触,不生锈 | 铜生锈 |
span>
(实验结论)铜生锈的条件是_____。
(反思与拓展)
(1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)如果要除去铜制品表面的铜锈,可以用稀盐酸浸泡,写出反应的化学方程式_____。
【答案】氧化铜、水和二氧化碳 ![]() 铜与水、氧气、二氧化碳等物质充分接触 除去水中溶解的氧气
铜与水、氧气、二氧化碳等物质充分接触 除去水中溶解的氧气 ![]()
【解析】
探究活动一:
[实验结论]
根据实验现象:绿色固体变为黑色,可知生成氧化铜;硫酸铜粉末变为蓝色,可知有水生成;烧杯中澄清石灰水变浑浊,说明生成二氧化碳;故加热铜锈生成的物质有:氧化铜、水和二氧化碳;
黑色固体即氧化铜,加入适量稀硫酸,稍加热溶解,溶液变为蓝色,反应生成硫酸铜和水,反应的方程式为:![]() 。
。
探究活动二:
[实验结论]
根据4个对比试验可知,一段时间后,只有实验4中的铜丝生锈了,说明铜生锈的条件是:铜与水、氧气、二氧化碳等物质充分接触;
[反思与拓展]
(1)水中能溶解少量的氧气,实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其目的是除去水中溶解的氧气。
(2)铜锈Cu2(OH)2CO3与稀盐酸反应生成氯化铜、水和二氧化碳,反应的化学方程式![]() 。
。

【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为________g
(2)该黄铜中铜的质量分数为多少_______?(写出计算过程)
(3)第三次实验后所得溶液的溶质为__________。