题目内容
【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为________g
(2)该黄铜中铜的质量分数为多少_______?(写出计算过程)
(3)第三次实验后所得溶液的溶质为__________。
【答案】0.2 67.5% 硫酸锌、硫酸
【解析】
(1)根据质量守恒定律,第一次加入20g稀硫酸,生成氢气的质量为:20g+20g-39.92g=0.08g,第二次加入20g稀硫酸,生成氢气的质量为:20g+40g-59.84g=0.16g,第三次加入20g稀硫酸,生成氢气的质量为:20g+60g-79.80g=0.2g,第四次加入20g稀硫酸,生成氢气的质量为:20g+80g-99.80g=0.2g,所以黄铜粉末完全反应生成氢气的总质量为0.2g。
(2)设该黄铜中铜的质量为x。
![]()
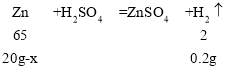
![]() ,解得x=13.5g
,解得x=13.5g
黄铜中铜的质量分数为:![]() ×100%=67.5%
×100%=67.5%
(3)根据分析可知,第三次实验时稀硫酸有剩余,所得溶液的溶质有生成的硫酸锌、剩余的硫酸。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
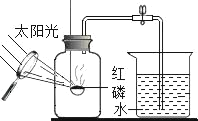
【题目】科学贵在创新,以下是对部分化学实验的改进,其中不能达到目的是( )
A | B | |
改 进 后 实 验 |
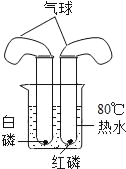
燃烧条件 |
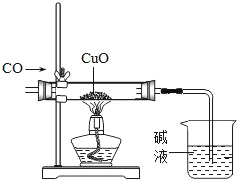
CO还原氧化剂 |
目的 | 防止燃烧产物污染空气 | 防止尾气对大气的污染 |
C | D | |
改 进 后 实 验 |
测定氧气含量 |
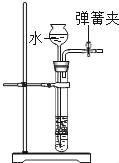
检验气密性 |
目的 | 不用酒精灯点燃,使测定结果更精确 | 现象更明显 |
A. AB. BC. CD. D