题目内容
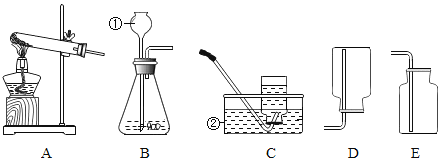
【题目】下图是同学们在实验室中完成“粗盐中难溶性杂质的去除”的实验,并用所得的氯化钠固体配制50g 16%的氯化钠溶液的主要操作。
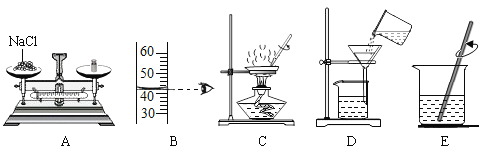
(1)若配制50g 16%的氯化钠溶液实验,需要上述操作中的____(填字母)
(2)若用量筒量取水时,仰视读数,导致配制溶液中溶质的质量分数会____(填“偏大”、“偏小”或“不变”)。
(3)操作C中玻璃棒搅拌的目的是____。
(4)操作D中有一处明显的错误,请改正____。
【答案】ABE 偏小 防止局部温度过高造成液滴飞溅 应用玻璃棒引流
【解析】
(1)若配制50g 16%的氯化钠溶液实验,需要称量、溶解操作,AB 是称量,E是溶解,故填:ABE。
(2)若用量筒量取水时,仰视读数,量取的液体体积偏大,导致配制溶液质量偏大,则溶质的质量分数会偏小,故填:偏小。
(3)操作C是蒸发操作,其中玻璃棒搅拌的目的是防止局部温度过高造成液滴飞溅。
(4)过滤操作中应该用玻璃棒引流,防止液体飞溅。

 快乐5加2金卷系列答案
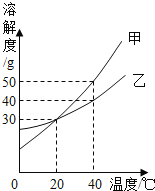
快乐5加2金卷系列答案【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是

A.将甲、乙的饱和溶液从t2℃分别降温到t1℃,析出晶体的质量甲一定大于乙 |
B.t1℃时甲、乙的饱和溶液中溶质质量分数相等 |
C.t2℃时将40g甲溶于100g水中,形成饱和溶液 |
D.将M点的甲溶液变成饱和溶液常采取的方法是__________________________。 |
【题目】“五一”假期,聪聪同学和家人到安徽省博物馆去参观,发现博物馆内许多铜制品表面有一层绿色物质。绿色物质是什么?它是怎样形成的?化学活动课上,同学们设计实验对这种绿色物质进行了如下探究活动。
(査阅资料)
①铜在空气中易生成铜锈,它为绿色,其主要成分是Cu2(OH)2CO3;
②白色的硫酸铜粉末遇水能变为蓝色。
探究活动一:验证铜锈的组成。
(进行实验1)
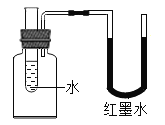
同学们设计了如图所示装置并进行实验。
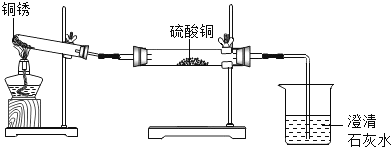
实验操作 | 实验现象 | 实验结论 |
①按如图组装仪器,装入药品。 ②加热铜锈,直至不再有气体产生,停止加热 | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊 | 加热铜锈生成的物质有_____; |
③冷却后,向试管中固体加入适量稀硫酸,稍加热 | 黑色固体溶解,溶液变为蓝色 | 发生反应的化学方程式为:_____。 |
探究活动二:探究铜生锈的条件。
(进行实验2)
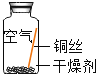
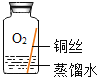
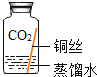
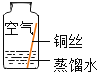
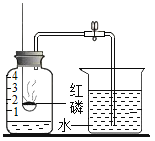
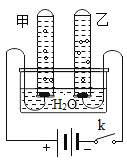
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
序号 | 实验1 | 实验2 | 实验3 | 实验4 |
实验内容 |
|
|
|
|
实验现象 | 在干燥环境中,铜不生锈 | 铜仅与氧气和水接触,不生锈 | 铜仅与二氧化碳和水接触,不生锈 | 铜生锈 |
span>
(实验结论)铜生锈的条件是_____。
(反思与拓展)
(1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)如果要除去铜制品表面的铜锈,可以用稀盐酸浸泡,写出反应的化学方程式_____。
【题目】下图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中不符合图示关系的是
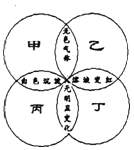
甲 | 乙 | 丙 | 丁 | |
A | Na2CO3 | H2SO4 | BaCl2 | 紫色石蕊 |
B | (NH4)2SO4 | NaOH | Ba(NO3)2 | 无色酚酞 |
C | K2CO3 | HCl | Ba(OH)2 | 紫色石蕊 |
D | HCl | Na2CO3 | AgNO3 | 无色酚酞 |
【题目】下表是NaOH和Ca(OH)2的溶解度数据,请回答下列问题.
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度(g) | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
(1)从表中数据可以获得的信息是__________(写一条).
(2)把80℃时NaOH的饱和溶液降温至20℃,可以看到的现象是__________,此时溶液的溶质质量分数为__________.(保留一位小数)
(3)某兴趣小组对部分变质的氢氧化钠固体进行提纯,设计了如下操作流程:请回答:

(Ⅰ)步骤②中加入过量Ca(OH)2的目的是__________;涉及反应的化学方程式为__________.
(Ⅱ)滤液B中的溶质是__________(写化学式);步骤③所包含的具体操作是加热浓缩、__________、过滤.
(Ⅲ)若实验前称得样品的质量为10g,实验后称得“滤渣A”和“NaOH固体”的质量分别是5g和8.7g,则此样品的纯度为__________.