3.化学平衡状态的判定
|
例 举 反 应 |
m
A(g) + n B(g)  p C(g) + q D(g) p C(g) + q D(g) |
|
|
混合物体系中各成分的含量 |
各物质的
物质的量或各物质的质量分数一定 |
平衡 |
|
各物质的质量或物质的质量分数一定 |
平衡 |
|
|
各气体的体积或体积分数一定 |
平衡 |
|
|
总体积、总压强、总物质的量一定 |
不一定平衡 |
|
|
正、逆反应速率相等 |
在单位时间内消耗了m mol A,同时也生成了m mol A,即v(正)=v(逆) |
平衡 |
|
在单位时间内消耗了n mol B,同时也消耗了p mol C,即v(正)=v(逆) |
平衡 |
|
|
v(A): v(B): v(C):
v(D)=m:n:p:q,v(正)不一定等于v(逆) |
不一定平衡 |
|
|
在单位时间内生成了n mol B,同时也消耗了p mol C,因均指v(逆) |
不一定平衡 |
|
|
压强 |
m + n ≠ p + q 时,总压强一定(其他条件一定) |
平衡 |
|
m + n = p + q 时,总压强一定(其他条件一定) |
不一定平衡 |
|
|
混合气体的平均相对分子质量M r |
M r一定时,且m + n ≠ p + q时(非气体的不算) |
平衡 |
|
M r一定时,且m + n = p + q时(非气体的不算) |
不一定平衡 |
|
|
温度 |
任何化学反应都伴有能量的变化,当体系温度一定时(其他不变) |
平衡 |
|
气体的密度 |
密度一定 |
不一定平衡 |
|
颜色 |
反应体系内有色物质的颜色稳定不变 |
平衡 |
注意:“同边异,异边同”原理(平衡的判断方法之一)
同一边的物质(都是反应物或者都是生成物)一个“消耗”一定量,同时另一个“生成”一定量才可以说明是达到了平衡;而两个不同一边的物质(一个是反应物而另一个是生成物)都“同时消耗”一定量或者“同时生成”一定量也可以表示达到了平衡。
[例1]对可逆反应A2(g)+B2(g) 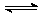 2AB(g) 在一定条件下,达到平衡状态的标志是( )
2AB(g) 在一定条件下,达到平衡状态的标志是( )
A、平衡时容器内各物质的物质的量比为1∶1∶2
B、平衡时容器内的总压强不随时间而变化
C、单位时间内生成2n mol AB的同时,生成n mol的B2
D、单位时间内,生成n mol A2的同时,生成n mol的B2
[解析] 平衡时容器内各物质的物质的量之比是没有规律的,只是各物质的物质的量浓度保持不变是一般规律,A错;对于反应前后气体不变的反应,容器内的总压强不随时间的变化而改变,无论是否平衡!B不能选择;对于C,D 类型需要了解六个字的“同边异,异边同”原理,对于D,如果反应向左进行,单位时间内,本来就是生成n mol A2的同时,一定生成了n mol的B2;对于C,表示反应向左进行的同时也在向右进行,而且程度相同!所以是正确的。
[答案]C
[方法技巧]“同边异,异边同”原理是一个很实用的原理,在学习中要灵活利用!
考点2化学平衡的影响因素及勒沙特列原理
 CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )