30.(15分)金属是现代生活和工业生产中应用极为普遍的一类材料。
 (1)已知在相同的条件下,金属的活动性越强,金属和酸反应
(1)已知在相同的条件下,金属的活动性越强,金属和酸反应
产生气泡(氢气)的速度就越快。Al、Cu、Fe三种金属在稀
盐酸里的反应现象如右图所示。
①右图中Y所代表的金属是 (填“Cu”或“Fe”);
②Al、Cu、Fe三种金属的活动性由强到弱的顺序为 ;
③铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是
;
(2)金属的开发和利用是人类文明和社会进步的标志。
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800 ℃左右,即可得到与黄金外观相似的“药金”。
I.用上述方法不能制得真正的黄金(Au)是因为 ;
II.“药金”是 (填“纯金属”或“合金”);
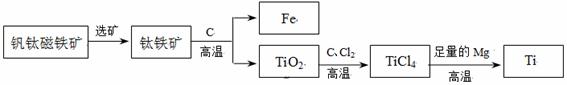 ②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”。由钒钛磁铁矿提取金属钛的主要工艺过程如下:
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”。由钒钛磁铁矿提取金属钛的主要工艺过程如下:
I.TiCl4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
。
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入_________________除去。
(3)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究。
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应。
①请完成证明金属粉末中存在Fe和Cu的实验设计:
|
实验操作 |
实验现象 |
结论 |
|
I.取少量的金属粉末于试管中,加入足量的 (填试剂名称)。 |
|
仅除去铝 |
|
II.将试管静置,弃去上层清液,加入足量的稀硫酸。 |
|
证明含有铁 |
|
III.将试管静置,弃去上层清液,加水,多次洗涤剩余固体 |
剩余固体呈紫红色 |
证明含有铜 |
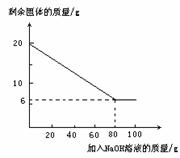 ②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与图象如下:
②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与图象如下:
|
加NaOH溶液的次数 |
第一次 |
第二次 |
第三次 |
… |
|
剩余固体的质量/g |
1 6.5 |
n |
9.5 |
… |
I.分析以上数据可知,上表中n的值为 ;
II.该金属粉末中Al的质量分数为 %
III.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
29.(7分)长途运输鱼苗时,常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
[提出问题]当把过氧化钙投入足量水中时,最终生成什么物质?
[进行猜想]甲同学:生成氧化钙和氧气; 乙同学:生成氢氧化钙和氧气。
同学和老师都认为甲同学的猜想是错误的,其理由是 ;
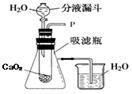 [实验探究]
[实验探究]
(1)打开右图装置中分液漏斗的活塞,控制滴加水速度,观察到
试管内有气泡产生。
① (填实验操作),
说明生成的气体是氧气。
②实验过程中,发现烧杯中有气泡出现,该现象说明 。
(2)请设计一个实验方案来验证过氧化钙和水反应产生的另一种物质是氢氧化钙:
|
实验步骤及操作方法 |
预期的实验现象 |
结论 |
|
①取少量过氧化钙放入试管中,加足量水,振荡, ② 。 |
①
产生气泡, ② 。 |
过氧化钙和水反应产生的另一种物质是氢氧化钙 |
[问题讨论]
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是 ;
(2)过氧化钙和水反应的化学方程式为 。
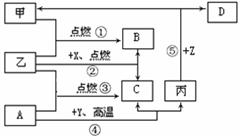 (3分)找规律(用化学符号填空):
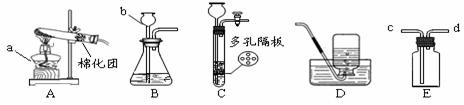
(3分)找规律(用化学符号填空):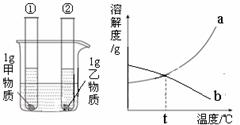 (4分)如图所示,烧杯中盛装20℃的水,试管①中盛装甲物质的溶液,试管②中盛装乙物质的溶液,且两试管中各有1g未溶解的固体(两支试管预先均经过充分振荡)。当两支试管中溶液的温度由20℃升到80℃时,发现试管①中甲固体消失,而试管②中的乙固体增加。
(4分)如图所示,烧杯中盛装20℃的水,试管①中盛装甲物质的溶液,试管②中盛装乙物质的溶液,且两试管中各有1g未溶解的固体(两支试管预先均经过充分振荡)。当两支试管中溶液的温度由20℃升到80℃时,发现试管①中甲固体消失,而试管②中的乙固体增加。