30、Ⅰ、第29届奥运会于2008年8月在我国北京举行。下面分别是一位运动员在一段时间内的血液中所含乳酸浓度(表1)和获胜的三位运动员所需的大约氧气量(表2)。
表1
|
时间(分) |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
50 |
55 |
60 |
|
血液中乳酸浓度(mg/cm3) |
5 |
5 |
5 |
40 |
70 |
100 |
80 |
60 |
40 |
35 |
25 |
23 |
20 |
表2
|
赛事(米) |
最高速度(km/h) |
赛事中吸收的氧气量(升) |
赛事中需要的氧气量(升) |
|
100 |
37 |
0.5 |
10 |
|
1500 |
25 |
18 |
36 |
|
10000 |
21.5 |
132 |
150 |
(1)从表1来看,进行运动的时间段为 ;运动员血液中正常的乳酸浓度是 ;人体产生乳酸的场所是 。 运动员从运动开始到运动后,期间血浆PH值变化趋势是 , 原因是
。
(2)氧债是指赛事后需要吸入的额外氧气量,以补偿赛事中所缺乏的氧气。从表2来看,人体能累积的最大氧债是 升。
(3)当人体进行剧烈运动时,会产生大量的热量,此时的体温是由位于 的体温中枢调控的。
(4)当人体进行剧烈运动后维持血糖稳定的主要生理调节过程是:
。
 Ⅱ、图1是用光学显微镜观察马蛔虫(2N=4)某器官切片所绘制的四个细胞分裂示意图;图2表示该动物某器官内不同分裂时的细胞中三种结构或物质的相对数量。请据图回答以下问题:
Ⅱ、图1是用光学显微镜观察马蛔虫(2N=4)某器官切片所绘制的四个细胞分裂示意图;图2表示该动物某器官内不同分裂时的细胞中三种结构或物质的相对数量。请据图回答以下问题:
⑴由图1判断,该切片取自马蛔虫的 (器官),其中细胞①内染色体、染色单体及核DNA分子的数量之比是 。含有同源染色体的细胞是 ,含有两个染色体组的细胞是 。
⑵图2中a、b、c所代表的三种结构或物质依次是 。图2中由②到③时期,三种物质或结构数量变化的原因是 。
⑶图1中的 细胞处于图2中的③所示时期,细胞名称是 。
26.(18分)类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2,为验证该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分。探究过程如下:
(1)提出假设:A是FeCl3,B是FeCl2
(2)设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同。请填写下表中的相应空格:
|
实验方法 |
实验现象 |
结论 |
|
分别向A、B溶液中加KSCN溶液 |
|
固体物质中有FeCl3 |
|
分别向KMnO4溶液中加适量A、B溶液 |
KMnO4溶液颜色无明显变化 |
固体物质中不含______ |
(3)根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式:
___________________________________________________。
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是
_____________(填写序号)
A.将A溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeCl3 、FeCl2、CuCl2,其离子方程式为_________________________。某研究性学习小组的同学们设计了两种从废液中回收Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤,在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜。该方案中涉及的四种阳离子的氧化性由强到弱的顺序为:
______________________________________。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,当观察到阴极上少量气泡产生时,即停止电解,这时要回收的Cu已全部析出,该方案中铜作________极。所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)
___________________________________________。
方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:
___________________________________________。

 (20分)如图所示,质量为M的平板车P高h,质量为m的小物块Q的大小不计,位于平板车的左端,系统原来静止在光滑水平面地面上.一不可伸长的轻质细绳长为R,一端悬于Q正上方高为R处,另一端系一质量也为m的小球(大小不计).今将小球拉至悬线与竖直位置成60°角,由静止释放,小球到达最低点时与Q的碰撞时间极短,且无机械能损失,已知Q离开平板车时速度大小是平板车速度的两倍,Q与P之间的动摩擦因数为μ,M:m=4:1,重力加速度为g.求:
(20分)如图所示,质量为M的平板车P高h,质量为m的小物块Q的大小不计,位于平板车的左端,系统原来静止在光滑水平面地面上.一不可伸长的轻质细绳长为R,一端悬于Q正上方高为R处,另一端系一质量也为m的小球(大小不计).今将小球拉至悬线与竖直位置成60°角,由静止释放,小球到达最低点时与Q的碰撞时间极短,且无机械能损失,已知Q离开平板车时速度大小是平板车速度的两倍,Q与P之间的动摩擦因数为μ,M:m=4:1,重力加速度为g.求: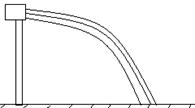 (9分)物理学是很实用的一门学科,在工农业生产中有许多运用。请你用所学的物理知识帮助农民测出水泵的流量(在单位时间内通过流管横截面的流体的体积称为流量)。已知水泵的出水管是水平的,且出水管外径在10cm左右。提供的实验器材有:一把钢卷尺、游标卡尺、螺旋测微器、一长直细木棒和一重锤线。
(9分)物理学是很实用的一门学科,在工农业生产中有许多运用。请你用所学的物理知识帮助农民测出水泵的流量(在单位时间内通过流管横截面的流体的体积称为流量)。已知水泵的出水管是水平的,且出水管外径在10cm左右。提供的实验器材有:一把钢卷尺、游标卡尺、螺旋测微器、一长直细木棒和一重锤线。
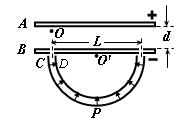
 (8分)(1)在用电流场模拟静电场描绘电场等势线的实验中,给出下列器材,应选用的是__________(用字母表示)
(8分)(1)在用电流场模拟静电场描绘电场等势线的实验中,给出下列器材,应选用的是__________(用字母表示)