网址:http://m.1010jiajiao.com/timu3_id_327466[举报]
NH4++AlO2-+H2O=Al(OH)3↓+NH3↑
试回答:(1)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少.
请答出各种现象由先到后出现的顺序(用序号回答)
(2)写出滴入NaOH溶液的过程中,有关反应的离子方程式:①
试回答:
(1)硫酸铝铵在水溶液中的电离方程式为
(2)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少.
请回答出各种现象由先到后出现的顺序(用序号回答)
(3)写出(2)小题中滴入NaOH溶液的过程中有关反应的离子方程式:
①
在某化工生产中,要用到一种无色、可溶于水的晶体--铝铵矾.该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵.向该复盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化.
试回答:
(1)硫酸铝铵在水溶液中的电离方程式为______.
(2)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少.
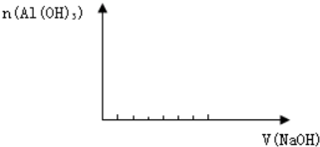
请回答出各种现象由先到后出现的顺序(用序号回答)______.并在下图中画出氢氧化钠的加入体积与沉淀量的关系:
(3)写出(2)小题中滴入NaOH溶液的过程中有关反应的离子方程式:
①______.②______.⑤______.
查看习题详情和答案>>
在某化工生产中,要用到一种无色、可溶于水的晶体——铝铵矾.该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵.向该复盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化.
已知NH4+与AlO2-在水溶液中不能大量共存,会发生反应:NH4++AlO2-+H2O![]() Al(OH)3↓+NH3↑.试回答:
Al(OH)3↓+NH3↑.试回答:
(1)硫酸铝铵在水溶液中的电离方程式为________;
(2)在逐滴加入浓NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀 ②有刺激性气味的气体产生 ③白色沉淀量逐渐增多 ④白色沉淀完全消失 ⑤白色沉淀量逐渐减少
请答出各种现象,由先到后出现的顺序(用序号回答)________;
(3)依次写出滴入NaOH溶液的过程中有关反应的离子方程式:
①________;
②________;
③________.
| |||||||||||||||