(1)小明在做“研究温度对反应速率的影响”实验时,他取了两只试管,均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于凉水中,记录溶液褪色所需的时间。
①需要用 来酸化KMnO4溶液,褪色所需时间tA tB(填“>”、“=”或“<”).
②写出该反应的离子方程式 .
(2)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol?L﹣1KMnO4溶液装入
(填“酸式”或“碱式”)滴定管,进行滴定操作。在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。请解释原因: 。当 ,证明达到滴定终点.
③计算:再重复上述操作2次,记录实验数据如下.
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 21.10 |
④误差分析:下列操作会导致测定结果偏高的是 。
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.不小心将少量酸性KMnO4溶液滴在锥形瓶外
E.观察读数时,滴定前仰视,滴定后俯视.
(12分)某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。请你帮助该同学整理并完成实验报告:
| 实验方案 | 实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成小球,在水面上游动,随之消失,溶液变红 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 | (B)产生气体,可在空气中燃烧,溶液变为浅红色 |
| ③钠与滴有酚酞试液的冷水反应 | (C)反应不十分强烈,产生的气体可在空气中燃烧 |
| ④镁带与2mol/L盐酸反应 | (D)剧烈反应,产生可燃气体 |
| ⑤铝条与2mol/L盐酸反应 | (E)生成白色胶状沉淀,后来沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | (F)生成淡黄色沉淀 |
(2) 实验用品:
仪器: ①________②________③________④ 试管夹 ⑤ 镊子 ⑥ 小刀 ⑦ 玻璃片⑧ 砂纸等;
药品:钠、镁带、铝条、2mol/L的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等。
(3) 实验内容:(填写与实验方案相对应的实验现象)
①______②______③______④______⑤______⑥______(用A-F表示)
(4) 实验结论:
金属性: ________________ 非金属性: ________________
(5)写出⑥的总反应离子方程式:_________________________________。
(12分)为回收和利用废旧塑料减轻“白色污染”,某兴趣小组进行如下探究:
| 实验课题 | 探究废旧塑料热分解的主要产物为多种烃的混合物 |
| 查阅资料 | ①CuO能将烃氧化成CO2和H2O; ②甲苯可被酸性KMnO4溶液氧化为苯甲酸,苯甲酸能溶于苯。 |
| 实验设计 |   |
| 实验记录 | 按上图连接装置,隔绝空气强热装置A中的试管(忽略装置内空气的影响),一段时间后,可观察到如下现象: ①B装置试管中有液态物质生成; ②C中溴水的颜色变浅; ③E中黑色氧化铜变红; ④F中无水硫酸铜变蓝。 |
(1)写出一定条件下制备聚丙烯化学方程式 。
(2)经分析得知装置B试管中的液态产物是甲苯和苯的混合物。设计实验除去其中含有的甲苯 。
(3)实验中装置C的作用是 。
(4)若没有装置D,对实验结论产生的影响是 。
(5)有同学认为“E中黑色氧化铜变红,F中无水硫酸铜变蓝”是废旧聚丙烯塑料热分解产物中含氢气导致的。请你在F装置后增加一个实验装置,以确认使CuO变红是气态烃,而不是氢气,将增加的装置图(要注明其中盛放的试剂名称)画在虚线框内。





 Na2S2O3(aq) (III)
Na2S2O3(aq) (III)

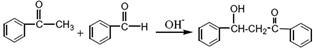
 (查尔酮)
(查尔酮)