(14分)某研究性学习小组在网上收集到如下信息:硫化钠,俗称臭碱,是一种强还原剂,在工业上用途广泛。他们对硫化钠与次氯酸钠的反应进行探究。
【实验】
在次氯酸钠溶液中加入硫化钠溶液,发现溶液始终澄清。
(1)下列有关硫化钠的说法正确的是 。
a. 硫化钠溶液不宜久置,应现用现配
b. 硫化钠溶液中通入SO2有淡黄色浑浊,可证明SO2有氧化性
c. 硫化钠在空气中潮解并不断放出H2S气体,说明酸性:H2CO3>H2S
d. 配制硫化钠溶液时加入少量氢氧化钾
e. 向硫化钠溶液中滴加稀硝酸有臭鸡蛋气味的气体生成
【提出假设】
(2)反应后的溶液中肯定存在Cl-、SO42-和OH-,为探究溶液中可能还存在的其他阴离子(不考虑离子水解及空气中CO2的影响),该学习小组提出如下假设:
假设1:只还存在S2-
假设2:只还存在ClO-
假设3:
【设计实验方案,验证假设】
(3)请写出实验步骤以及预期现象和结论。
限选实验试剂:1 mol? L-1的CuSO4溶液、1 mol? L-1NaOH溶液、淀粉-KI溶液、紫色石蕊试液、酚酞试液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少许反应后溶液于试管中,滴加 | 若 ,则假设 成立。 |
| 步骤:2:另取少许反应后溶液于试管中,滴加 | 若 ,则假设 成立。 若 , 则假设3成立。 |
【思考与交流】
(4)实验时某同学发现所用硫化钠溶液呈黄色,联想到工业盐酸呈黄色的原因,该同学认为所用硫化钠溶液中混有少量FeCl3。你是否同意该同学的的观点 (填“同意”或“不同意”),请简述理由: 。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液 | B.升华 | C.结晶 | D.分液 E.蒸馏 F.层析 G.过滤 |
(2)__ _从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)__ _分离水和汽油的混合物。
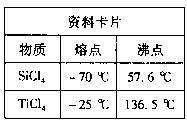
(4)__ _分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
②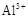 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全;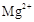 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 | 实验操作 | 实验现象 |
| I | 向X的粉末中加入过量盐酸 | 产生气体A,得到无色溶液 |
| II | 向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 | 生成白色沉淀B |
| III | 向沉淀B中加过量NaOH溶液 | 沉淀全部溶解 |
| IV | 向II得到的滤液中滴加NaOH溶液,调节pH至12 | 生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是 。
(2)II中生成B反应的离子方程式是 。
(3)III中B溶解反应的离子方程式是 。
(4)沉淀C的化学式是 。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是 。

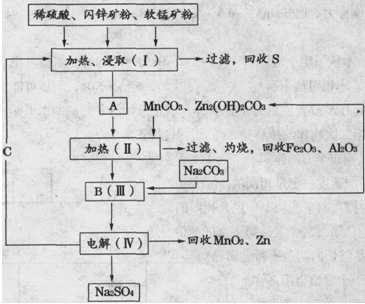
 MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。