下图为某化工厂用石墨电解Na2CrO4溶液制备Na2Cr2O7的模拟装置,下列有关说法错误的是:
| A.溶液中OH-由阴极区流向阳极区 |
| B.阳极区产生的气体与阴极区产生的气体在相同状况下体积之比为1:2 |
| C.阳极的电极反应式为:2H2O-4e-=O2↑+4H+ |
| D.Na2CrO4转化为Na2Cr2O7的离子方程式为:2CrO42-+2H+= Cr2O72-+H2O |
镁锰干电池的电化学反应式为:Mg+2MnO2+H2O  Mg(OH)2+Mn2O3。下列说法不正确的是:
Mg(OH)2+Mn2O3。下列说法不正确的是:
| A.镁为负极,发生氧化反应 |
| B.可以选择碱性溶液作为电解质 |
| C.反应后正极和负极附近溶液的pH均升高 |
D.正极的电极反应为:2MnO2+H2O+2e- Mn2O3+2OH- Mn2O3+2OH- |
以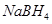 (B元素的化合价为+3)和
(B元素的化合价为+3)和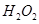 为原料的电池,可以作为通讯卫星的高能电池。其电极负极材料为Pt/C,正极材料为
为原料的电池,可以作为通讯卫星的高能电池。其电极负极材料为Pt/C,正极材料为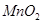 ,工作原理如图所示。下列说法不正确的是
,工作原理如图所示。下列说法不正确的是
| A.该电池工作时Na+由a极区移向b极区 |
| B.电极b是原电池的正极 |
C.该电池的负极反应为: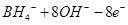 = =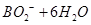 |
D.电路中通过6.02×1022个电子时,理论上消耗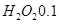 mol mol |
全世界每年钢铁因锈蚀造成大量的损失。某城市拟用如图方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀。关于此方法,下列说法不正确的是
| A.土壤中的钢铁易被腐蚀是因为在潮湿的土壤中形成了原电池 |
| B.金属棒M的材料应该是比镁活泼的金属 |
C.金属棒M上发生反应: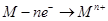 |
| D.这种方法称为牺牲阳极的阴极保护法 |
下列有关实验现象的描述中,正确的是
A.如图所示装置中,锌电极上一定没有气泡生成 |
| B.向CaCl2饱和溶液中通入少量CO2,溶液中会出现白色沉淀 |
| C.做氯化铵分解实验时,加热试管底部,试管口处有晶体出现 |
| D.向蛋白质溶液中滴加足量饱和NaCl溶液的过程中无固体析出 |
铅蓄电池的反应原理为:2PbSO4+2H2O Pb+PbO2+2H2SO4,下列叙述中,正确的是
Pb+PbO2+2H2SO4,下列叙述中,正确的是
| A.PbSO4的氧化性比PbO2的强、还原性比Pb的强 |
| B.放电时,PbO2为氧化剂、做负极,Pb为还原剂、做正极 |
| C.放电时,当有2 mol H2SO4反应时,会有1.204×1024个电子从铅电极流出 |
| D.充电时,PbSO4既被氧化又被还原,Pb是阳极产物之一 |
LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的应用前景。已知该电池放电时的电极反应式为:
正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+,下列说法中正确的是
| A.充电时阳极反应为Li++e-=Li |
| B.充电时动力电池上标注“-”的电极应与外接电源的负极相连 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上是Li+得电子被还原 |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是
| A.电流从右侧电极经过负载后流向左侧电极 |
| B.负极发生的电极反应式为:N2H4 + 4OH- - 4e - = N2+ 4H2O |
| C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D.该燃料电池持续放电时,正极发生氧化反应,PH减小 |
铅蓄电池的两极分别为Pb、PbO2,电解液为硫酸,工作时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下面结论正确的是( )。
| A.Pb为正极,被氧化 |
| B.溶液的pH不断减小 |
C.S 只向PbO2处移动 只向PbO2处移动 |
| D.电解液密度不断减小 |
关于化学电源的叙述,错误的是( )。
| A.化学电源均是根据原电池的工作原理设计的 |
| B.在干电池中,碳棒只起导电作用,并不参加化学反应 |
| C.镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵 |
| D.燃料电池是一种高效、环保的新型化学电源 |