题目内容
镁锰干电池的电化学反应式为:Mg+2MnO2+H2O  Mg(OH)2+Mn2O3。下列说法不正确的是:
Mg(OH)2+Mn2O3。下列说法不正确的是:
| A.镁为负极,发生氧化反应 |
| B.可以选择碱性溶液作为电解质 |
| C.反应后正极和负极附近溶液的pH均升高 |
D.正极的电极反应为:2MnO2+H2O+2e- Mn2O3+2OH- Mn2O3+2OH- |
C
解析试题分析:镁锰干电池的电化学反应式为Mg+2MnO2+H2O═Mg(OH)2+Mn2O3,分析可知镁失电子发生氧化反应,做负极,故A正确;镁锰干电池的电化学反应式为:Mg+2MnO2+H2O═Mg(OH)2+Mn2O3,负极电极反应为Mg-2e-+2OH-=Mg(OH)2,电解质溶液为碱性溶液,故B正确;负极镁失电子生成的镁离子和氢氧根结合生成氢氧化镁沉淀,Mg-2e-+2OH-=Mg(OH)2,氢氧根离子浓度减小,正极电极反应2MnO2+H2O+2e-═Mn2O3+2OH-过程中生成氢氧根离子,所以正极附近溶液pH增大,负极附近溶液pH减小,故C错误;正极是MnO2得到电子发生还原反应生成Mn2O3,正极的电极反应为2MnO2+H2O+2e-═Mn2O3+2OH-,故D正确;故选C。
考点:考查原电池原理的分析应用。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的应用前景。已知该电池放电时的电极反应式为:
正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+,下列说法中正确的是
| A.充电时阳极反应为Li++e-=Li |
| B.充电时动力电池上标注“-”的电极应与外接电源的负极相连 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上是Li+得电子被还原 |
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 
| A.a处通入氧气 |
| B.b处为电池正极,发生了还原反应 |
| C.该装置中只涉及两种形式的能量转化 |
| D.P-型半导体连接的是电池负极 |
已知蓄电池在放电时起原电池的作用,在充电时起电解池的作用。汽车上用的铅蓄电池是以一组充满海绵状灰铅的铅板和另一组结构相似的充满二氧化铅的铅板组成。两个电极用稀硫酸作电解质溶液。在放电时,两极发生的反应可分别表示为:
Pb+S-2e- PbSO4
PbSO4
PbO2+4H++S+2e- PbSO4+2H2O
PbSO4+2H2O
充电时,两极发生的反应分别表示为:
PbSO4+2e- Pb+S
Pb+S
PbSO4+2H2O-2e- PbO2+4H++S
PbO2+4H++S
则在放电时,下列说法中正确的是( )
| A.充满海绵状灰铅的铅板为电源正极 |
| B.充满二氧化铅的铅板为电源负极 |
| C.铅板在放电时发生氧化反应 |
| D.铅板在放电时发生还原反应 |
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图。下列说法正确的是( )
| A.镁作Y电极 |
| B.电池工作时,Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
| D.X电极上发生的反应为ClO-+2H2O-4e-=ClO3-+4H+ |
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融)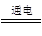 4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH
4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH 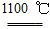 Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
| A.电解熔融氢氧化钠制钠,阳极发生的电极反应为2OH--2e-=H2↑+O2↑ |
| B.若用戴维法与吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| C.吕萨克法制钠的原理是利用铁的还原性比钠强 |
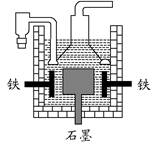
| D.目前工业上常用电解熔融氯化钠法制钠(如下图),电解槽中石墨为阳极,铁为阴极 |
下列有关电化学知识的描述正确的是 ( )
| A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
如图所示,?为直流电源,?为浸透饱和氯化钠溶液和酚酞试液的滤纸,?为电镀槽。接通电路(未闭合K)后发现?上的c点显红色。为实现铁片上镀铜,接通K后,使c、d两点短路。下列叙述不正确的是( )。
| A.b为直流电源的负极 |
| B.f极为阴极,发生还原反应 |
| C.e极材料为铁片,f极材料为铜片 |
| D.可选用CuSO4溶液或CuCl2溶液作电镀液 |
 B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。
B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。