将标准状况下1.12L氨气溶于500mL水中配制成溶液,从中取出5mL,有关这5mL溶液的叙 述正确的是
| A.溶液中c(NH4+)< c(OH—) | B.氨水的物质的量浓度为0.1 mol·L—1 |
| C.溶液的pH>13 | D.与5mL 0.1mol·L—1HCl溶液恰好完全中和 |
0.1 mol·L—1NH4Cl溶液的pH最接近于
| A.13 | B.7 | C.5.2 | D.1 |
将下列气体通入水中,其饱和水溶液酸性最强的是
| A.CH4 | B.NH3 | C.HBr | D.SO2 |
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-)。下列说法正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B.a 点可表示MnCO3的饱和溶液,且c(Mn2+)= c(CO32-) |
| C.b 点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c 点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-) |
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
| | ① | ② | ③ | ④ |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B.分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
室温下向10 mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目增加,导电性增强 |
| B.醋酸的电离程度增大,c(H+)亦增大 |
| C.再加入10 m L pH="11" NaOH溶液,混合液pH=7 |
D.溶液中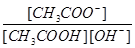 不变 不变 |
下列事实可证明氨水中的(NH3?H2O)是弱碱的是
| A.氨水能被弱酸醋酸中和 | B.铵盐受热易分解 |
| C.氨水可以使酚酞试液变红 | D.常温下,0.1 mol/L氯化铵溶液的pH约为5 |
已知Ksp(AgCl) =1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12 。在只含有KCl、K2CrO4的混合溶液中滴加0.001000 mol/L的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×l0-3 mo l/L,此时溶液中Cl-的物质的量浓度是
| A.8. 90×10-6 mol/L | B.1. 36×10-5 mol/L |
| C.1×10-5mol/L | D.4. 45×10-2mol/L |
如图所示是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线。下列说法正确的是
| A.水电离出的氢离子浓度:a>b |
| B.盐酸的物质的量浓度为:0.010 0 mol·L-1 |
| C.指示剂变色时,说明盐酸与NaOH恰好完全反应 |
| D.当滴加NaOH溶液10.00 mL时(忽略反应前后体积变化),该混合液的pH=1+lg 3 |