题目内容
在常温下,下列有关溶液中微粒的物质的量浓度关系正确的是
A.1L0.1mol·L-1(NH4)2Fe(SO4)2·6H2O的溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH—)+c (SO42—)
B.0.1 mol·L-1 NH4HS溶液中:c(NH4+)<c(HS-)+c(H2S)+c(S2-)
C.0.1mol·L-1pH为4的NaHA溶液中:c(HA-)>c(H2A)>c(A2-)
D.等浓度的碳酸钠和碳酸氢钠溶液混合后的溶液中:c(OH-)+c(CO32-)=c(HCO3-)+c(H2CO3)+c(H+)
B
解析试题分析:A、根据电荷守恒可知,1L0.1mol·L-1(NH4)2Fe(SO4)2·6H2O的溶液中:c(NH4+)+2c(Fe2+)+c(H+)=c(OH—)+2c (SO42—),A不正确;B、根据物料守恒可知0.1 mol·L-1 NH4HS溶液中:c(NH3·H2O)+c(NH4+)=c(HS-)+c(H2S)+c(S2-),因此c(NH4+)<c(HS-)+c(H2S)+c(S2-),B正确;0.1mol·L-1pH为4的NaHA溶液说明HA-的电离程度强于HA-的水解程度,所以溶液中c(HA-)>c(A2-)>c(H2A),C不正确;D、等浓度的碳酸钠和碳酸氢钠溶液混合后的溶液中根据电荷守恒可知c(OH-)+2c(CO32-)+c(HCO3-)=c(Na+)+c(H+)。根据物料守恒可知2c(Na+)=3c(H2CO3)+3c(CO32-)+3c(HCO3-),则溶液中2c(OH-)+c(CO32-)=c(HCO3-)+3c(H2CO3)+2c(H+),D不正确,答案选B。
考点:考查溶液中离子浓度大小比较以及离子浓度关系的正误判断

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案水是一种极弱的电解质,在室温下,KW=1×10-14,则此时水的电离百分数为:
| A.1×10-7 | B.1/55.6 | C.10-14 | D.1/(55.6×107) |
下列比较中,正确的是
| A.同温和同物质的量浓度时,HF比HCN易电离,则溶液pH:NaF>NaCN |
| B.物质的量浓度相等的H2S和NaHS混合溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C.0.1mol/L的醋酸溶液加水稀释,c(H+)、c(OH-)同比例减小 |
| D.体积相同、pH相同的NH4Cl溶液、盐酸,完全溶解少量且等量的锌粉,前者用时长 |
已知Ksp(AgCl) =1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12 。在只含有KCl、K2CrO4的混合溶液中滴加0.001000 mol/L的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×l0-3 mo l/L,此时溶液中Cl-的物质的量浓度是
| A.8. 90×10-6 mol/L | B.1. 36×10-5 mol/L |
| C.1×10-5mol/L | D.4. 45×10-2mol/L |
常温下测得浓度均为0.1 mol·L—1的下列三种溶液的pH:
| 溶 质 | NaHCO3 | Na2CO3 | NaCN |
| pH | 8.4 | 11.6 | 11.1 |
下列说法中错误的是
A.溶液中阳离子物质的量之和的关系为:Na2CO3>NaHCO3=NaCN
B.相同条件下的酸性:H2CO3>HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度会使c(HCO3—)/ c(CO32—)增大
相同温度下等物质的量浓度的下列溶液中,pH值最大的是
| A.NH4Cl | B.NH4HCO3 | C.NH4HSO4 | D.(NH4)2SO4 |
常温下,pH=12的氢氧化钠溶液pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
| A.混合前的醋酸约1%发生电离 | B.混合后的溶液中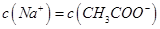 |
| C.氢氧化钠和醋酸和浓度不相等 | D.混合后的溶液呈中性 |
25 ℃时,Kw =1.0×10-14;100 ℃时,Kw =5.5×10-13。下列说法正确的是( )
| A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 |
| B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 |
| C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L CH3COOH恰好中和,所得溶液的pH="7" |
| D.25 ℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
 H++B2-,则下列说法中一定正确的是
H++B2-,则下列说法中一定正确的是