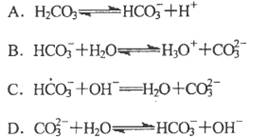
对“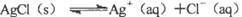 ”的理解正确的是( )。
”的理解正确的是( )。
| A.说明AgCl没有完全电离,AgCl是弱电解质 |
| B.说明溶解的AgCl已完全电离,AgCl是强电解质 |
| C.说明Ag+与Cl-的反应不能完全进行到底 |
| D.说明Ag+与Cl-的反应可以完全进行到底 |
把Ca(OH)2放入蒸馏水中,一段时间后达到如下平衡:

 ,下列说法正确的是( )
,下列说法正确的是( )
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
下列液体均处于25℃,下列有关叙述正确的是( )
| A.PH值相同的盐酸和氯化铵溶液中水的电离程度相同 |
| B.某溶液中由水电离出的c(H+)=10-13,则该溶液的PH一定为13 |
| C.PH=4.5的番茄汁中c(H+)是PH=6.5的牛奶中c(H+)的2倍 |
| D.中和浓度和体积均相同的盐酸和醋酸,消耗的氢氧化钠的物质的量之比为1:1 |
下列说法正确的是( )
| A.常温下,醋酸钠与醋酸的混合溶液PH=7,C(Na+)>c(CH3COO-) |
| B.0.1mol/LNa2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| C.将PH=6的H2SO4稀释1000倍后,c(H+)=2c(SO42-) |
| D.0.1mol/LNaHCO3溶液中:c(Na+)+c(H+)= c(HCO3-)+ c(OH-)+2c(CO32-) |
能说明0.1 mol·L-1的NaHA溶液一定呈酸性的是( )
①稀释时,溶液中c(OH-)增大
②溶液的pH<7
③溶液中c(Na+)=c(A2-)
④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
| A.①②④ | B.①③④ | C.①③ | D.②④ |
250C时,0.1mol·L-1稀醋酸加水稀释,如图中的纵坐标y可以是( )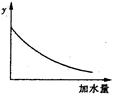
| A.溶液的pH | B.醋酸的电离平衡常数 |
| C.溶液的导电能力 | D.醋酸的电离程度 |
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O  CH3COO- + H3O+ CH3COO- + H3O+ |
B.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
D.Br- + H2O  HBr + OH- HBr + OH- |
25℃时,浓度均为1 mol/L的AX、BX、AY、BY四种正盐溶液,AX溶液的pH=7且溶液中c(X-)=1 mol/L,BX溶液的pH=4,BY溶液的pH=6。下列说法正确的是( )
| A.AY溶液的pH小于7 |
| B.AY溶液的pH小于BY溶液的pH |
| C.稀释相同倍数,BX溶液的pH变化小于BY溶液 |
| D.电离平衡常数K(BOH)小于K(HY) |