题目内容
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O  CH3COO- + H3O+ CH3COO- + H3O+ |
B.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
D.Br- + H2O  HBr + OH- HBr + OH- |
B
解析试题分析:A、是醋酸电离的方程式,错误;B、是铵根离子水解的方程式,正确;C、碳酸是二元弱酸,水解时是分步进行的,以第一步水解为主,应该是:CO32- + H2O HCO3- + OH-,错误;D、溴离子不会发生水解,错误。
HCO3- + OH-,错误;D、溴离子不会发生水解,错误。
考点:考查离子的水解。

练习册系列答案
相关题目
常温下,向l00mL0.01mol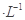 HA溶液中逐滴加入0.02mol
HA溶液中逐滴加入0.02mol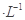 MOH溶液,如图所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是:
MOH溶液,如图所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是: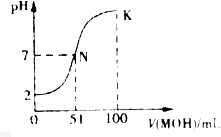
| A.HA为一元强酸 |
| B.MOH为一元弱碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.若K点对应的溶液的PH=10,则有c(MOH)+ c(OH-)- c(H+)=0.005mol/L |
常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全中和,则下列说法错误的是
| A.氨水的浓度等于盐酸的浓度 |
| B.原氨水中有1%的含氮微粒为NH4+ |
| C.氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D.混合溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=5×10-4mol·L-1 |
把Ca(OH)2放入蒸馏水中,一段时间后达到如下平衡:

 ,下列说法正确的是( )
,下列说法正确的是( )
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
为探究某种盐的水解是吸热反应。有四位同学分别设计了如下实验方案:
| 同学 | 实验设计 |
| 甲 | 将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的 |
| 乙 | 加热能使溶液中的Fe3+转化成Fe(OH)3沉淀,说明Fe3+水解是吸热的 |
| 丙 | 通过实验发现同浓度的热的纯碱溶液比冷的纯碱溶液去油污效果好,说明碳酸钠水解是吸热的 |
| 丁 | 在醋酸钠溶液中滴入酚酞试液,加热(不考虑水蒸发)后若红色加深,说明醋酸钠水解是吸热的 |
其中不正确的是( )
A.甲 B.乙 C.丙 D.丁
25℃时,将a mol·L-1一元酸HA与b mol·L-1 NaOH等体积混合后测得溶液pH=7,则下列关系一定不正确的是( )
| A.a=b | B.a>b |
| C.c(A-)=c(Na+) | D.c(A-)<c(Na+) |
咖喱是一种烹饪辅料,白色衬衣被咖喱汁玷污后,用普通肥皂洗涤,发现黄色污渍变成红色,经水漂洗后红色又变成黄色。与咖喱汁具有上述相似化学原理的试剂有( )
| A.石蕊试液 | B.品红试液 | C.氯水 | D.淀粉KI(aq) |
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/mol·L-1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=
 mol·L-1
mol·L-1C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是( )
| A.HA可能为一元弱酸 |
| B.MOH为一元强碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.若K点对应的溶液的pH=10,则有c(MOH)+c(M+)="0.01" mol·L-1 |