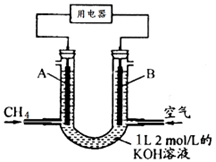
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是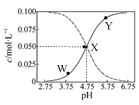
| A.Y点所表示的溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol·L-1 |
| C.该温度下醋酸的电离平衡常数为10—4.75 mol·L-1 |
| D.向X点所表示的溶液中加入等体积的0.05 mol·L-1 NaOH溶液 :c(H+)=c(CH3COOH)+c(OH-) |
下列说法不正确的是
| A.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
| B.加热、蒸发MgCl2饱和溶液可得无水MgCl2晶体 |
| C.工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 |
| D.室温下,c(NH4+)相等的(NH4)2SO4、NH4HCO3、NH4Cl溶液中:c(NH4)2SO4<c(NH4Cl)<c(NH4HCO3) |
室温下,0.1mol·L-1CH3COONa溶液与 0.1 mol·L-1NaCl溶液等体积混合(忽略溶液体积变化),下列有关叙述正确的是
| A.混合前CH3COONa溶液中由水电离出来的c(OH—)>1×10-7 mol·L-1 |
| B.混合前NaCl溶液中:c(Na+) + c(OH—)= c(Cl-)+c(H+) |
| C.混合溶液中 :c(Cl-) >c(CH3COOH) >c(OH—) |
| D.混合溶液中:c(Cl-) + c(CH3COO-) =0.1mol·L-1 |
下列说法不正确的是
| A.NaHCO3和Na2CO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| B.常温下,浓度均为0.1 mol·L-1下列各溶液的pH:NaOH>Na2CO3> NaHCO3> NH4Cl |
| C.向冰醋酸中逐滴加水,醋酸的电离程度、pH均先增大后减小 |
| D.常温下,pH=1的稀硫酸与醋酸溶液中,c(SO42-)与c(CH3COO-)之比为2∶1 |
室温下,将一元酸HA溶液和NaOH溶液等体积混合,实验数据如表:
| 实验编号 | 起始浓度c(HA) | 起始浓度c(NaOH) | 反应后溶液的pH |
| ① | 0.1 mol·L-1 | 0.1 mol·L-1 | 9 |
| ② | x | 0.2mol·L-1 | 7 |
下列说法正确的是
A.实验①反应前HA溶液中c(H+)=c(OH-)+ c(A-)
B.实验①反应后溶液中c(A-)>c(Na +)
C.实验②反应前HA溶液浓度x>0.2 mol·L-1
D.实验②反应后溶液中c(A-)+ c(HA)= c(Na+)
常温时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.饱和碳酸钠溶液中:c(Na+)= 2c(CO32-)+ 2c(HCO3-)+2c(H2CO3) |
| B.pH=2的醋酸中:c(H+)=0.02mol?L-1 |
| C.0.1 mol?L-1氯化铵溶液中:c(H+)> c(OH-)> c(Cl-)> c(NH4+) |
| D.pH=12的NaOH溶液与等体积0.01 mol·L-1氯化铵溶液混合后所得溶液中:c(Na+) = c(NH4+) |
H2S水溶液中存在电离平衡H2S H++HS-和HS-
H++HS-和HS- H++S2-。若向H2S溶液中
H++S2-。若向H2S溶液中
| A.滴加新制氯水,溶液pH减小 | B.通入过量SO2气体,溶液pH增大 |
| C.加水,溶液中氢离子浓度增大 | D.加入少量硫酸铜固体,所有离子浓度都减小 |
物质的量浓度相同的下列溶液中,含离子和分子种类最多的是
| A.CaCl2 | B.CH3COONa |
| C.氨水 | D.K2S |
下列反应不属于水解反应或水解方程式不正确的是
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液:HCO3-+H2O=CO32-+H3O+
⑤NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
| A.①②③④ | B.①②③ |
| C.②③⑤ | D.全部 |