下列有关水的叙述正确的是
| A.水是一种非电解质 |
| B.纯水中c(H+)随着温度的升高而降低 |
| C.由液态水结成冰的过程是一个熵增的过程 |
| D.25℃,pH相同的氢氧化钠溶液与醋酸钠溶液,水的电离度前者小于后者 |
下列过程或现象与盐类水解无关的是
| A.纯碱溶液去油污 | B.加热稀醋酸溶液其pH 稍有减小 |
| C.明矾净水 | D.浓的硫化钠溶液有臭鸡蛋气味 |
常温下,0.1mol·L-1CH3COONa溶液中,微粒浓度间关系正确的是
| A.c(Na+)=c(CH3COO-) >c(OH-)=c(H+) |
| B.c(OH-)=c(H+)+ c(CH3COOH) |
| C.c(Na+) + c(H+)= c(CH3COO-) +c(OH-) |
| D.c(CH3COOH) + c(CH3COO-) = c(Na+)+ c(H+) |
己知25℃时,Ksp(AgCl) =1.8×10-10,Ksp(AgBr) =5.4×10-13,Ksp(AgI) =8.5×10-17。某溶液中含有C1-、Br-和I-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.C1-、Br-、I- | B.Br-、C1-、I- |
| C.I-、Br-、C1- | D.Br-、I-、C1- |
下列事实中,能说明HNO2是弱电解质的是
| A.用HNO2溶液做导电性实验,灯泡较暗 |
| B.HNO2是共价化合物 |
| C.HNO2溶液不与NaCl反应 |
| D.室温下,0.1mol·L-1 HNO2溶液的pH为2.15 |
下列说法正确的是
| A.向蒸馏水中滴加浓H2SO4时,KW不变 |
| B.常温下,0.005mol·L-1Ba(OH)2溶液pH为12 |
C.Na2CO3水解的离子方程式为:CO32- + 2H2O H2CO3+ 2OH- H2CO3+ 2OH- |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
25℃时,将0.1mol·L-1氨水溶液加水稀释,下列数值变大的是
| A.c(OH-) | B.pH | C.c(NH4+)/c(NH3·H2O) | D.c(H+)·c(OH-) |
下列说法正确的是
| A.常温下,某溶液中由水电离出的c(H+)=1×10-amo1·L–1,若a<7时,则该溶液可能为NaHSO4溶液 |
| B.常温下,中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸)=V(醋酸) |
| C.25℃时,已知Ka(CH3COOH)=1.7×10-5mo1·L–1、Ka(C6H5OH) =1.0×10-10mo1·L–1、 Ka1(H2CO3) = 4.2×10-7mo1·L–1 、Ka2(H2CO3) =5.6×10-11mo1·L–1pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| D.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加入稀盐酸有气泡产生,说明常温下Ksp(BaSO4)>Ksp(BaCO3) |
常温下,已知0.1mol·L-1的CH3COOH和HCN溶液的PH分别为a、b,且1<a< b。下列有关叙述不正确的是( )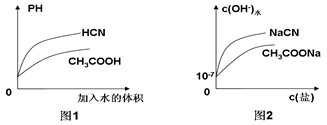
| A.常温下,等浓度的CH3COONa溶液和NaCN溶液的PH前者较小 |
| B.在NaCN溶液中:c (Na+)+ c (H+) =c (OH-)+ c (CN-) |
| C.相同温度下,相同PH的CH3COOH和HCN溶液分别加水稀释,溶液PH随溶液体积变化的曲线如图1所示 |
| D.常温下,CH3COONa溶液和NaCN溶液中由水电离出的c(OH-)与盐浓度的变化曲线如图2所示 |
下列叙述中,正确的是
A.用惰性电极电解 溶液分别得到单质 溶液分别得到单质 和Cl2 和Cl2 |
B.常温下,某溶液中由水电离出的 ,该溶液一定呈酸性 ,该溶液一定呈酸性 |
C. 溶液和 溶液和 溶液加热蒸干、灼烧都得到 溶液加热蒸干、灼烧都得到 |
| D.在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |