下列反应中产生气泡速率最快的是
| | 温度 | 浓度 | 催化剂 |
| A | 25℃ | 2mL5%H2O2 | 0.1mol/LFeCl32滴 |
| B | 35℃ | 2mL8%H2O2 | MnO2粉末 |
| C | 25℃ | 2mL5%H2O2 | MnO2粉末 |
| D | 25℃ | 2mL8%H2O2 | 0.1mol/LCuCl22滴 |
PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生反应,在10 min时达到平衡:PCl3(g)+Cl2(g) PCl5(g)。有关数据如下:
PCl5(g)。有关数据如下:
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
下列判断错误的是
A.10 min内,v(Cl2)=0.04 mol/(L·min)
B.当反应达到平衡时,容器中Cl2为1.2 mol
C.若升高温度反应的平衡常数减小,则平衡时PCl3的转化率变大
D.平衡后再加入2.0 mol PCl3,在相同条件下再达平衡时,c(PCl5)<1.0mol/L
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应: SO2(g)+NO2(g) SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示。则正确的结论是
SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示。则正确的结论是
| A.逆反应速率:a点小于点c |
| B.反应物浓度:a点小于点b |
| C.反应在c点时SO2的转化率最大 |
| D.反应物的总能量低于生成物的总能量 |
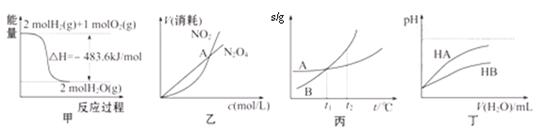
下列图示与对应的叙述相符的是 ( )
图1 图2 图3 图4
| A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示0.1000 mol·L-1NaOH溶液滴定20.00mL0.1000 mol·L-1CH3COOH溶液所得到的滴定曲线 |
| C.图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的饱和溶液 |
| D.图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正 > v逆 |
(双选)在1 L密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-Q kJ·mol-1(Q>O),容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) △H=-Q kJ·mol-1(Q>O),容器内部分物质的物质的量浓度如下表:
 浓度 浓度时间 | c(NH3) (mol/L) | c(O2 ) (mol/L) | c(NO) (mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
| 第10min | 0.7 | 1.475 | 0.1 |
A.反应在第2 min到第4min时,O2的平均反应速率为0.1875 mol/(L·min)
B.反应在第2 min时改变了某一条件,该条件可能是使用催化剂或升高温度
C.第4 min时、第8 min时分别达到化学平衡,且平衡常数不相同
D.在开始反应的前2 min内,该反应的△H=-0.05Q kJ·mol-1
难挥发性二硫化担(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:
下列说法正确的是
| A.该反应的△H>0 |
| B.在提纯过程中,S2的量不断增加 |
| C.该反应的平衡常数与I2的浓度成正比 |
| D.经过足够长时间后,石英管右端将得到纯净的TaS2 |

 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
 pC(g)+qD(g) ΔH<0。下列结论中错误的是
pC(g)+qD(g) ΔH<0。下列结论中错误的是
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态