对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是( )
①升高温度;②改用100mL 3mol/L盐酸;③多用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
| A.①③④⑤ | B.①②④⑤ | C.①②③④ | D.①②④ |
下列说法正确的是
| A.增大体系压强,活化分子数增加,化学反应速率一定增大 |
| B.加入反应物,使活化分子百分数增加,化学反应速率增大 |
| C.活化分子间所发生的分子间的碰撞均为有效碰撞 |
| D.升高温度,活化分子百分数增加,化学反应速率一定增大 |
下列关于化学反应速率的说法正确的是( )
| A.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| B.化学反应速率为0.8mol/(L·s)是指1s时某物质的浓度为0.8mol/L |
| C.化学反应速率是指一定时间内反应物的物质的量减少或生成物的物质的量增加 |
| D.对于任何化学反应来说,反应速率越大,反应现象就越明显 |
在恒温、容积为2 L的密闭容器中充入2 mol SO2和一定量O2。发生反应2SO2+O2? ?2SO3,当反应进行到4 min时,测得n (SO2)=0.4 mol。若反应进行到2 min时,容器中SO2的物质的量是( )
?2SO3,当反应进行到4 min时,测得n (SO2)=0.4 mol。若反应进行到2 min时,容器中SO2的物质的量是( )
| A.等于1.6 mol | B.等于1.2 mol |
| C.大于1.6 mol | D.小于1.2 mol |
对于密闭容器中的可逆反应:4L(g)  2M(g)+N(g) △H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示。图中y轴是指
2M(g)+N(g) △H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示。图中y轴是指
| A.气体混合物的平均相对分子质量 |
| B.气体混合物的总物质的量浓度 |
| C.L在气体混合物的体积分数 |
| D.气体混合物的密度 |
设C+CO2  2CO(正反应为吸热反应),反应速率为υ1;N2+3H2
2CO(正反应为吸热反应),反应速率为υ1;N2+3H2 2NH3(正反应为放热反应),反应速率为υ2,对于上述反应,当温度升高时,υ1和υ2的变化情况为
2NH3(正反应为放热反应),反应速率为υ2,对于上述反应,当温度升高时,υ1和υ2的变化情况为
| A.同时增大 | B.同时减小 | C.υ1增大,υ2减小 | D.υ1减小,υ2增大 |
下列事实中,不能用勒夏特列原理解释的是
| A.密闭、低温是存放氨水的必要条件 |
| B.实验室常用排饱和食盐水法收集氯气 |
| C.硝酸工业生产中,使用过量空气以提高NH3的利用率 |
| D.合成氨反应采用较高温度和使用催化剂,以提高氨气的产量 |
判断反应过程自发性的目的
| A.判断反应的方向 | B.确定反应是否一定发生 |
| C.判断反应过程发生的速率 | D.判断反应过程的热效应 |
已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)  H2(g)+I2(g)的化学平衡常数为
H2(g)+I2(g)的化学平衡常数为
| A.50 | B.0.02 | C.100 | D.无法确定 |
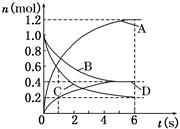
 6A+2D
6A+2D