题目内容
下列关于化学反应速率的说法正确的是( )
| A.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| B.化学反应速率为0.8mol/(L·s)是指1s时某物质的浓度为0.8mol/L |
| C.化学反应速率是指一定时间内反应物的物质的量减少或生成物的物质的量增加 |
| D.对于任何化学反应来说,反应速率越大,反应现象就越明显 |
A
解析试题分析:反应速率即化学反应进行的快慢,单位为mol/(L·s)或mol/(L·min)。即单位时间内反应物的浓度的减少或生成物浓度的增加量。浓度单位一般用mol/L,时间单位用秒、分或小时。化学反应并非均匀速率进行:反应速率分为平均速率(一定时间间隔里平均反应速率)和瞬时速率(给定某时刻的反应速率),可通过实验测定。D选项中,很多反应无现象。故D错误。
考点:化学反应速率定义

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
图为某化学反应速率一时间图。在 时刻升高温度或增大压强,都符合下图所示变化的反应是
时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2(g)+O2(g) 2SO3(g);ΔH<0 2SO3(g);ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g);ΔH<0 4NO(g)+6H2O(g);ΔH<0 |
C.H2(g)+I2(g) 2HI(g); ΔH>0 2HI(g); ΔH>0 |
D.C(s)+H2O(g) CO(g)+H2(g) ;ΔH>0 CO(g)+H2(g) ;ΔH>0 |
对于可逆反应:aA(g)+bB(g) mC(g)+ nD(g);△H<0,下列说法正确的是
mC(g)+ nD(g);△H<0,下列说法正确的是
| A.浓度改变平衡必移动 | B.增大压强平衡必移动 |
| C.升高温度平衡必移动 | D.导入氦气平衡必移动 |
下列事实不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率 |
判断反应过程自发性的目的
| A.判断反应的方向 | B.确定反应是否一定发生 |
| C.判断反应过程发生的速率 | D.判断反应过程的热效应 |
下列变化过程中,ΔS<0的是
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl |
| C.干冰的升华 | D.CaCO3(S)分解为CaO(S)和CO2(g) |
在密闭容器中,反应X2(g)+Y2(g) 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )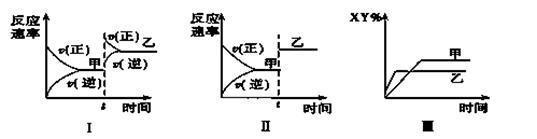
| A.图Ⅰ是增大压强的变化情况 |
| B.图Ⅱ是一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强或升高温度的变化情况 |
| D.图Ⅲ一定是升高温度的变化情况 |
今有X(g)+Y(g)  2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
| A.增大X或Y的浓度 | B.增大压强 |
| C.增大Z的浓度 | D.升高温度 |
 zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是