题目内容
下列事实中,不能用勒夏特列原理解释的是
| A.密闭、低温是存放氨水的必要条件 |
| B.实验室常用排饱和食盐水法收集氯气 |
| C.硝酸工业生产中,使用过量空气以提高NH3的利用率 |
| D.合成氨反应采用较高温度和使用催化剂,以提高氨气的产量 |
D
解析试题分析:如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,中这就是勒夏特列原理,该原理适用于所有的平衡体系。A、温度越低,气体的溶解度越大,物质分解的速率越小,所以密闭、低温是存放氨水的必要条件可以用勒夏特列原理解释,A不符合题意;B、氯气溶于水生成氯化氢和次氯酸,饱和食盐水中氯离子浓度大,可以抑制氯气的溶解,则实验室常用排饱和食盐水法收集氯气可以用勒夏特列原理解释,B不符合题意;C、硝酸工业生产中,使用过量空气,增大氧气的浓度促使平衡向正反应方向移动,所以提高NH3的利用率,可以用勒夏特列原理解释,C不符合题意;D、催化剂不能改变平衡状态,只能改变反应速率。合成氨是放热反应,低温有利于氨气的生成。所以合成氨反应采用较高温度和使用催化剂,以提高氨气的产量不能用勒夏特列原理解释,D正确,答案选D。
考点:考查勒夏特列原理应用的有关判断

COCl2(g)  CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
| A.①④⑥ | B.①②④ | C.②③⑥ | D.③⑤⑥ |
在一密闭容器中,反应aA(g) bB(g),达到平衡后,保持温度不变,将容器体积增加1倍,当达到新的平衡时,B的浓度是原来的70%,则
bB(g),达到平衡后,保持温度不变,将容器体积增加1倍,当达到新的平衡时,B的浓度是原来的70%,则
| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.化学计量数关系:a>b |
将等物质的量的F2和ClF混合,在密闭容器中发生反应:F2(g)+ClF(g) 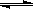 ClF3(g) ΔH<0。下列叙述正确的是
ClF3(g) ΔH<0。下列叙述正确的是
| A.保持恒容,平衡后再降低温度,平衡常数减小 |
| B.若增加F2的用量,平衡正向移动,则反应物的转化率均增大 |
| C.达到平衡后,若增大容器体积,则正反应速率减小,逆反应速率增大,平衡左移 |
| D.恒温恒容时,当ClF转化40%时,容器内的压强为初始时的0.8 |
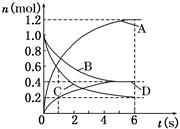
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列说法正确的是 
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为: X(g)+Y(g) Z(g) Z(g) |
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数相等
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①体积为0.5 L,则平衡时放出的热量<23.15 kJ
反应3X(g)+Y(g)  2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
| A.v(X)=0.05mol·L–1·min–1 | B.v(Z)=0.10mol·L–1·min–1 |
| C.v(Y)=0.10mol·L–1·min–1 | D.v(W)=0.05mol·L–1·min–1 |
 6A+2D
6A+2D