对于一可逆反应,当确知平衡向正反应方向移动,下列说法肯定正确的是
| A.反应物的转化率将提高 | B.生成物的产量将增加 |
| C.生成物的浓度将增大 | D.生成物的百分含量将增大 |
某温度下,X(g)+Y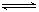 2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
| A.正反应是吸热反应,Z是固体 |
| B.逆反应是放热反应,Y是固体,Z为气体 |
| C.正反应是吸热反应,只有Z不是气体 |
| D.正反应是放热反应,Y和Z均为气体 |
可逆反应:A+3B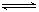 2C+2D(各物质均为气体),在不同情况下测得有下列4 种
2C+2D(各物质均为气体),在不同情况下测得有下列4 种
反应速率,其中反应最快的是
| A.vD=0.4 mol / (L·s) | B.v C=0.5 mol / (L·s) |
| C.v B=0.6 mol / (L·s) | D.v A=0.15 mol / (L·s) |
在一定温度下,可逆反应:A2(气)+B2(气) 2AB(气),达到平衡的标志是
2AB(气),达到平衡的标志是
| A.容器的总压强不随时间而变化 |
| B.单位时间内有n molA2生成的同时有n molB2生成 |
| C.单位时间内有n molB2发生反应的同时有n molAB分解 |
| D.单位时间内生成n molA2同时就有2n molAB生成 |
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.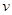 (W)=3 (W)=3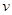 (Z) (Z) | B.2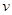 (X)=3 (X)=3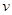 (Z) (Z) |
C.2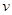 (X)= (X)=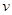 (Y) (Y) | D.3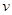 (W)=2 (W)=2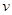 (X) (X) |
现有可逆反应A(g)+2B(g) nC(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是( )
nC(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是( )
| A.p1>p2,n>3 |
| B.p1<p2,n>3 |
| C.p1<p2,n<3 |
| D.p1>p2,n=3? |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
| A.a>b | B.a=b | C.a<b | D.无法确定 |
下列关于判断过程的方向的说法正确的是 ( )
| A.所有自发进行的化学反应都是放热反应 |
| B.判断化学反应能否自发进行,必须综合考虑反应的焓变和熵变 |
| C.自发反应一定是熵增大,非自发反应一定是熵减小的反应 |
| D.同一物质的固、液、气三种状态中固体的熵值最大 |
在100 ℃时,把0.5 mol N2O4通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol·L-1。在60 s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是 ( )
| A.前2 s以N2O4的浓度变化表示的反应速率为0.01 mol·L-1·s-1 |
| B.在2 s时体系内的压强为开始时的1.1倍 |
| C.在平衡时体系内含N2O4 0.25 mol |
| D.平衡时,N2O4的转化率为40% |
 B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是 ( )
B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是 ( )