题目内容
对于一可逆反应,当确知平衡向正反应方向移动,下列说法肯定正确的是
| A.反应物的转化率将提高 | B.生成物的产量将增加 |
| C.生成物的浓度将增大 | D.生成物的百分含量将增大 |
B
解析试题分析:A选项,若增大某一反应的浓度,平衡向正反应移动,其它反应物的转化率增大,自身转化率
降低,故A错误;B选项,平衡向正反应方向移动,生成物的产量一定增加,故B正确;C选项,如
在一定压强的密闭容器中,正反应是气体体积增大的反应,向容器中通入稀有气体,平衡向正反应方
向移动,但生成物浓度降低,故C错误;D选项,如增加反应物的物质的量,平衡向正方向移动,若
增加的多,转化的少,则生成物的百分含量反而减小,故D错误。
考点:化学平衡的影响因素

练习册系列答案
相关题目
下列说法中正确的是( )
| A.凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| B.自发反应在恰当条件下才能实现 |
| C.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
| D.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | H2O/ mol |
| 0 | 1.2 | 0.6 |
| t1 | 0.8 | |
| t2 | | 0.2 |
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)=0.4/t1 mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.6 molCO和1.2 molH2O,到达平衡时,c(CO2)=0.2 mol·L-1。
C.保持其他条件不变,向平衡体系中再通入0.6 mol H2O,与原平衡相比,达到新平衡时H2的体积分数增大
D.温度降至550℃,上述反应平衡常数为1.26,则正反应为吸热反应
现有可逆反应A(g)+2B(g) nC(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是( )
nC(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是( )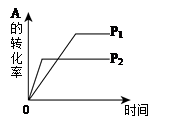
| A.p1>p2,n>3 |
| B.p1<p2,n>3 |
| C.p1<p2,n<3 |
| D.p1>p2,n=3? |
对于密闭容器中的反应:2SO2(g)+O2(g) 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是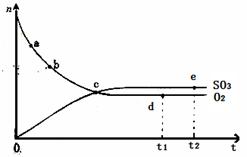
| A.点c处反应达到平衡 |
| B.点a的正反应速率比点b的大 |
| C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样 |
| D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的d点值要大 |
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) △H=-92.6kJ/moL。实验测得起始、平衡时数据如下表:
2NH3(g) △H=-92.6kJ/moL。实验测得起始、平衡时数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系 能量的变化 | ||
| N2 | H2 | NH3 | | |
| | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
下列事实中,不能用勒夏特列原理解释的是
| A.Fe(SCN)3,溶液中加入固体KSCN后颜色变深 |
| B.向稀盐酸中加入少量蒸馏水,盐酸中氯离子浓度降低 |
| C.实验室常用排饱和食盐水的方法收集氯气 |
| D.棕红色NO2。加压后颜色先变深后变浅 |
在下列平衡2CrO42-(黄色)+ 2H+ Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
| A.H+ | B.OH- | C.K+ | D.H2O |
下列事实不能用化学平衡原理解释的是
| A.温度控制在500℃有利于合成氨反应 |
| B.用排饱和食盐水法收集Cl2 |
| C.打开碳酸饮料会有大量气泡冒出 |
| D.在硫酸工业生产中使用过量的氧气 |