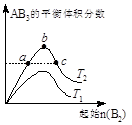将X和Y以1:2的体积比混合后置于密闭容器中,加压到3×107Pa,发生如下反应:X(g)+2Y(g)?2Z(g),达到平衡状态时,测得反应物的总物质的量和生成物的总物质的量相等,有关数据如图,则反应对应的温度是( )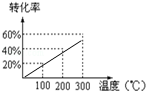
| A.100℃ | B.200℃ | C.300℃ | D.不能确定 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | H2O/ mol |
| 0 | 1.2 | 0.6 |
| t1 | 0.8 | |
| t2 | | 0.2 |
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)=0.4/t1 mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.6 molCO和1.2 molH2O,到达平衡时,c(CO2)=0.2 mol·L-1。
C.保持其他条件不变,向平衡体系中再通入0.6 mol H2O,与原平衡相比,达到新平衡时H2的体积分数增大
D.温度降至550℃,上述反应平衡常数为1.26,则正反应为吸热反应
将1.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,一定条件下发生反应:PCl3(g)+ Cl2(g) PCl5(g),达到平衡时PCl5为0.3mol·L-1,如果此时再充入1.0 molPCl3和1.0 mol Cl2,在相同温度下再达到平衡时,PCl5的物质的量浓度是
PCl5(g),达到平衡时PCl5为0.3mol·L-1,如果此时再充入1.0 molPCl3和1.0 mol Cl2,在相同温度下再达到平衡时,PCl5的物质的量浓度是
| A.0.6mol·L-1 | B.大于0.3 mol·L-1,小于0.6 mol·L-1 |
| C.大于0.6 mol·L-1 | D.小于0.3 mol·L-1 |
工业生产苯乙烯是利用乙苯的脱氢反应:
下列说法错误的是
| A.该反应中生成物的总能量高于反应物 |
| B.增大压强反应物活化分子百分数不变 |
| C.升高温度可以提高原料乙苯的转化率 |
| D.不断分离出苯乙烯可加快反应速率 |
硫代硫酸钠与稀盐酸的反应Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O在加热条件下反应速度加快,原因主要是
| A.该反应是吸热反应,且可逆,加热使平衡向正向移动 |
| B.加热促使SO2逸出,使平衡向正向移动 |
| C.加热促进S2O32-与H+的碰撞,使反应加速 |
| D.加热促进Na+与Cl-的碰撞,使反应加速 |
某可逆反应aA+bB cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
A.写成2aA+2bB 2cC,Q值、K值均扩大了一倍 2cC,Q值、K值均扩大了一倍 |
B.写成2aA+2bB 2cC,Q值扩大了一倍,K值保持不变 2cC,Q值扩大了一倍,K值保持不变 |
C.写成cC aA+bB,Q值、K值变为原来的相反数 aA+bB,Q值、K值变为原来的相反数 |
D.写成cC aA+bB,Q值变为原来的相反数,K值变为倒数 aA+bB,Q值变为原来的相反数,K值变为倒数 |
可逆反应:2NO2 2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是( )
2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是( )
| A.单位时间内生成n mol O2的同时生成2n mol NO2 |
| B.混合气体的密度不再改变的状态 |
| C.混合气体的颜色不再改变的状态 |
| D.混合气体的平均相对分子质量不再改变的状态 |
 2C(g) △H <0,下列各图正确的是( )
2C(g) △H <0,下列各图正确的是( )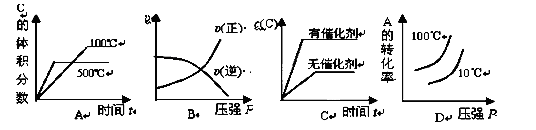
 2AB3(g)化学平衡状态的影响,得到如右图所示的变化规律(T表示温度)。下列结论正确的是
2AB3(g)化学平衡状态的影响,得到如右图所示的变化规律(T表示温度)。下列结论正确的是