题目内容
可逆反应:2NO2 2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是( )
2NO+O2在固定体积的密闭容器中反应,不能说明已达到化学平衡状态的是( )
| A.单位时间内生成n mol O2的同时生成2n mol NO2 |
| B.混合气体的密度不再改变的状态 |
| C.混合气体的颜色不再改变的状态 |
| D.混合气体的平均相对分子质量不再改变的状态 |
B
解析试题分析:
考点:考查化学平衡状态的判断。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.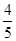 v(NH3)=v(O2) v(NH3)=v(O2) | B.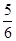 v(O2)=v(H2O) v(O2)=v(H2O) |
C.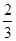 v(NH3)=v(H2O) v(NH3)=v(H2O) | D.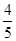 v(O2)=v(NO) v(O2)=v(NO) |
关于冰融化为水的过程判断正确的是]
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS>0 | C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS<0 |
恒容容器中反应:A(g)+3B(g) 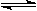 2C(g)+3D(g),达到平衡的标志是
2C(g)+3D(g),达到平衡的标志是
①体系的压强不再改变 ②混合气体的平均相对分子质量不再改变 ③各组分的浓度不再改变 ④混合气体的密度不变 ⑤反应速率vA: vB: vC: vD=1:3:2:3 ⑥单位时间内1 mol A断键反应,同时2 mol C也断键反应
| A.②③⑤⑥ | B.②③④⑤ | C.①④⑤⑥ | D.①②③⑥ |
对于反应2CO(g)+ O2(g) 2CO2(g)(正反应为放热反应),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡正向移动的是 ( )
2CO2(g)(正反应为放热反应),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡正向移动的是 ( )
| A.恒容通入少量He | B.恒容通入少量CO2 | C.升高温度 | D.缩小容器体积 |
工业生产苯乙烯是利用乙苯的脱氢反应:
下列说法错误的是
| A.该反应中生成物的总能量高于反应物 |
| B.增大压强反应物活化分子百分数不变 |
| C.升高温度可以提高原料乙苯的转化率 |
| D.不断分离出苯乙烯可加快反应速率 |
下列关于判断过程的方向的说法正确的是 ( )
| A.所有自发进行的化学反应都是放热反应 |
| B.判断化学反应能否自发进行,必须综合考虑反应的焓变和熵变 |
| C.自发反应一定是熵增大,非自发反应一定是熵减小的反应 |
| D.同一物质的固、液、气三种状态中固体的熵值最大 |
在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)
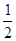 N2(g)+CO2(g);ΔH=-373.2kJ·mol-1
N2(g)+CO2(g);ΔH=-373.2kJ·mol-1
达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时减小压强 |
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是
| A.脱氢反应的△H<0 |
| B.600K时,Y点甲醇的υ(正) <υ(逆) |
| C.从Y点到Z点可通过增大压强 |
| D.在t1K时,该反应的平衡常数为8.1mol·L-1 |