下列有关说法正确的是
| A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| B.镀锌铁制品镀层受损后,铁制品比受损前更容易生锈 |
| C.生铁中含有碳,抗腐蚀能力比纯铁强 |
| D.Zn具有还原性和导电性,可用作碱性锌锰干电池的负极材料 |
已知:H2(g) +I2(g)  2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
| 起始浓度 | c(H2) / mol/L | c(I2) / mol/L | c(HI) / mol/L |
| 甲 | 0.01 | 0.01 | 0 |
| 乙 | 0.02 | 0.02 | 0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
已知2SO2 (g) + O2 (g)  2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
| A.容器内压强P:P甲=P丙 > 2P乙 |
| B.SO3的质量m:m甲=m丙 > 2m乙 |
| C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙 |
| D.反应放出或吸收热量的数值Q:Q甲=Q丙 > 2Q乙 |
mA(气) + nB(气) pC(气) + qQ(气)当m、n、p、q为任意整数时,下列情况一定是平衡状态的是:
pC(气) + qQ(气)当m、n、p、q为任意整数时,下列情况一定是平衡状态的是:
体系的压强不再改变
体系的温度不再改变
各组分的浓度不再改变
各组分的质量分数不再改变
反应速率Va:Vb:Vc:Vd=m:n:p:q
单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
在一密闭容器中,反应 aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质B的质量分数减小了 | D.a>b |
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 2C(g) ΔH < 0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是
2C(g) ΔH < 0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是
| A.0~t2时,v正>v逆 |
| B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ |
| C.t2时刻改变的条件可以是向密闭容器中加C |
| D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数I<Ⅱ |
在密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是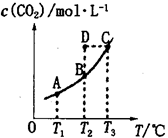
| A.平衡状态A与C相比,平衡状态A的c(CO)小 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
C.反应CO(g)+H2O(g) CO2(g)+H2(g)△H>0 CO2(g)+H2(g)△H>0 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
 xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是( )
xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是( )
 2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( )
2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( ) )
)