一定条件下,C0与H2反应可生成乙醇:2CO+4H2? CH3CH20H+H20。下列关于该反应的说法错误的是
| A.增大CO的浓度能减小反应速率 |
| B.升高体系温度能增大反应速率 |
| C.使用合适的催化剂可增大反应速率 |
| D.若反应在密闭容器中进行,H2和C0不能全部转化为产物 |
在容积可变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )
| A.图Ⅰ表示的是t1时刻升高温度对反应速率的影响 |
| B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 |
| D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
一定条件下,对于可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是( )
| A.c1 : c2=1 : 3 |
| B.平衡时,3VY (正) =2VZ (逆) |
| C.X、Y的转化率相等 |
| D.c1的取值范围为0.06<c1<0.16 mol/L |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) △H=Q kJ·mol-1;反应达到平衡时,X的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) △H=Q kJ·mol-1;反应达到平衡时,X的物质的量浓度与温度、气体体积的关系如下表所示:
| 容器体积/L c(X)/mol·L—1 温度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0. 90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
A.m>n
B.温度不变,增大体积,X的转化率增大
C.Q<0
D.体积不变,温度升高,平衡向正反应方向移动
在1L密闭容器中,把l mol A和1 mol B混合发生如下反应:
3A(g) + B(g)  XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是
XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是
| A.x的值为2 | B.A的转化率为40% |
| C.B的平衡浓度为0.8 mol/L | D.达到平衡时D的体积分数为20% |
一定条件下,可逆反应C(s)+CO2(g) 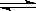 2CO(g) ΔH<0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
2CO(g) ΔH<0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
| A.①②③④ | B.①③ | C.②④ | D.①③④ |
在温度相同,压强分别为p1、p2条件下,A(g)+2B(g) nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是
nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是
| A.p1 > p2 n < 3 | B.p1< p2 n > 3 |
| C.p1< p2n = 3 | D.p1 > p2n > 3 |
下列事实可用勒夏特列原理解释的是
| A.使用催化剂有利于加快合成氨反应的反应速率 |
| B.硫酸工业中,将黄铁矿粉碎后加入沸腾炉中 |
| C.500℃左右比在室温时更有利于提高合成氨的转化率 |
| D.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 |
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
| A.平衡时,物质的量比A∶B∶C=2∶11∶4 |
| B.x值等于4 |
| C.B的平均反应速率为0.04 mol·L-1·min-1 |
| D.A的转化率20% |
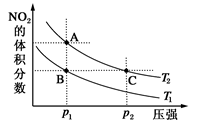
 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )